题目内容
5.某无色的混合气体可能含有NO2、NO、CO2、O2、NH3、N2中的几种,将100mL该气体经过如图所示的实验进行处理,结果得到酸性溶液,而几乎无气体剩余,有关该气体组成的判断不正确的是( )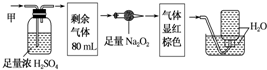
| A. | 一定含NH3,其体积为20mL | B. | 一定含CO2,其体积为48mL | ||
| C. | 一定含NO,其体积为30mL | D. | 该气体中一定不含NO2、N2、O2 |
分析 二氧化氮是红棕色的气体,浓硫酸可以和氨气反应,二氧化碳可以和过氧化钠反应生成碳酸钠和氧气,一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,氮气不溶于水.
解答 解:二氧化氮是红棕色的气体,所以一定不存在NO2,甲气体经过足量的浓硫酸,剩余气体80毫升,说明一定有NH3存在,二氧化碳可以和过氧化钠反应生成碳酸钠和氧气,一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,通过足量的过氧化钠后气体显红棕色,说明有NO、CO2,那么一定没有氧气;
排水法收集气体,广口瓶被上升的水注满,说明没有N2,
所以混合气体的组成可能为:NH3、NO、CO2,
A、据此分析可知,混合气体中一定含有氨气,且体积为20mL,故A正确;
B、得到酸性溶液为硝酸,反应为:4NO+3O2+2H2O=4HNO3,2Na2O2+2CO2=2Na2CO3+O2 ,故需满足:2CO2-O2-$\frac{4}{3}$NO,三者的体积总共为80mL,设二氧化碳的体积为2x,则有2x+$\frac{4}{3}$x=80,解x=24,即二氧化碳的体积为48mL,故B正确;
C、依据B的计算,NO体积为,故C错误;
D、依据分析可知,溶液中一定不含NO2、N2、O2,故D正确,故选C.
点评 本题考查常见气体的检验和性质,是一道气体的鉴别题目,题目难度中等,注意氨气的碱性、二氧化碳和过氧化钠的反应原理,明确常见气体的性质及检验方法为解答关键.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案
相关题目
15.在给定的四种溶液中,各离子能在该溶液中大量共存的是( )
| A. | 滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、SCN- | |
| B. | pH为1的溶液:Fe2+、K+、ClO-、Cl- | |
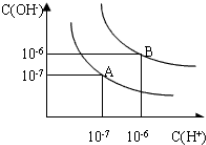
| C. | c(H+)=10-12 mol•L-1的溶液:K+、Ba2+、Cl-、NO3- | |
| D. | 存在较多的H+、SO42-、NO3-的溶液:Al3+、CH3COO-、Cl- |
13.检验机动车驾驶员是否“酒后驾驶”是利用橘黄色经硫酸酸化的CrO3溶液吸收乙醇,依据生成的绿色Cr3+的浓度来确定,其反应原理为CrO3+CH3CH2OH+H2SO4→Cr2(SO4)3+CH3CHO+H2O(未配平).下列说法正确的是( )
| A. | 该反应中CH3CH2OH表现氧化性 | |
| B. | 该反应发生氧化反应的过程是CrO3→Cr2(SO4)3 | |
| C. | 该反应中氧化产物与还原产物的物质的量之比为2:3 | |
| D. | 该反应中每生成1mol H2O转移1mol电子 |
20.分别将1g Na2CO3和1g NaHCO3装在两支试管中,各加入10mL水,振荡使它们溶解,冷却到室温后,分别向两支试管中滴入2滴酚酞.下列说法正确的是( )
| A. | 两支试管中的溶液都显红色,且Na2CO3溶液比NaHCO3溶液更红 | |
| B. | 两支试管中的溶液都显红色,且两者颜色没有区别 | |
| C. | 两支试管中的溶液都显蓝色,且Na2CO3溶液比NaHCO3溶液更蓝 | |
| D. | 两支试管中的溶液都不显颜色 |
10.β-羧乙基锗倍半氧化物(即Ge-132)是与人体健康有关的最重要的有机储化合物,其片层结构如图,每个结构相同的基团都是由六个锗原子和六个氧原子构成的十二元环,每个锗原子还同时与三个氧原子相连结,形成可以任意延伸的片层.在片层结构中,每个正六边形平均拥有的锗原子数与氧原子数各位( )

| A. | 6,6 | B. | 2,5 | C. | 2,3 | D. | 2,2 |
17.下列物质中,分子的一端亲水,分子的另一端亲油的是( )
| A. | CH3Cl | B. | 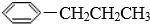 | C. | CH3(CH2)4COOCH3 | D. | CH3(CH2)13SO3Na |
14.下列有关胶体的叙述中不正确的是( )
| A. | 淀粉溶胶中胶体微粒直径大小在1~100nm | |
| B. | 用一束光照射氢氧化铁胶体,可以观察到一条光亮的通路 | |
| C. | 向烧杯中沸腾的蒸馏水里加几滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热可得氢氧化铁胶体 | |
| D. | 可以利用过滤操作来分离胶体粒子和溶液 |
15.氯仿 (CHCl3)不溶于水,密度比水大,是一种良好的有机溶剂,若保存不当受到光照射时,易被氧化而产生剧毒光气(COCl2),同时生成HCl,下列有关氯仿变质的检验正确的是( )
| A. | 用蒸馏水检验氯仿是否变质 | |
| B. | 用硝酸银溶液检验氯仿是否变质 | |
| C. | 用氢氧化钠检验氯仿是否变质 | |
| D. | 用干燥的蓝色石蕊试纸检验氯仿是否变质 |