题目内容
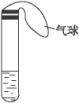
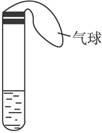
 某学生课外活动小组利用如图装置做如下实验:在试管中注入某无色溶液,加热试管,溶液颜色变为红色,冷却后恢复无色,则( )
某学生课外活动小组利用如图装置做如下实验:在试管中注入某无色溶液,加热试管,溶液颜色变为红色,冷却后恢复无色,则( )分析:二氧化硫能使品红溶液褪色,但二氧化硫的漂白性不稳定,加热时溶液又恢复原来的颜色,据此分析解答.
解答:解:A.二氧化硫和有色物质反应生成无色物质,但二氧化硫的漂白性不稳定,加热时溶液又恢复原来的颜色,所以溶有二氧化硫的品红溶液符合题意,故A正确;
B.氨气和水反应生成一水合氨,一水合氨电离出氢氧根离子而使溶液呈碱性,酚酞遇碱变红色,加热条件下,一水合氨易分解生成氨气而使溶液褪色,故B错误;
C.二氧化硫和水反应生成亚硫酸,酚酞在酸性溶液中为无色,二氧化硫不能使酸碱指示剂褪色,故C错误;
D.氯气和水反应生成次氯酸,次氯酸具有强氧化性而使品红溶液褪色,且次氯酸的漂白性具有不可逆性,故D错误;
故选A.
B.氨气和水反应生成一水合氨,一水合氨电离出氢氧根离子而使溶液呈碱性,酚酞遇碱变红色,加热条件下,一水合氨易分解生成氨气而使溶液褪色,故B错误;
C.二氧化硫和水反应生成亚硫酸,酚酞在酸性溶液中为无色,二氧化硫不能使酸碱指示剂褪色,故C错误;
D.氯气和水反应生成次氯酸,次氯酸具有强氧化性而使品红溶液褪色,且次氯酸的漂白性具有不可逆性,故D错误;
故选A.
点评:本题考查了二氧化硫的漂白性,知道二氧化硫漂白原理是解本题关键,注意二氧化硫与次氯酸、臭氧、木炭漂白性的差异,难度中等.

练习册系列答案
相关题目
 I向一金属铝的易拉罐内充满CO2,然后向罐内注入足量NaOH溶液,立即用胶布严封罐口,过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起,解释上述变化的实验现象:
I向一金属铝的易拉罐内充满CO2,然后向罐内注入足量NaOH溶液,立即用胶布严封罐口,过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起,解释上述变化的实验现象: