题目内容
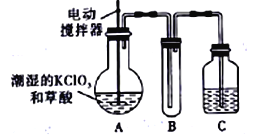
【题目】某溶液X中可能含有下列离子中的若干种:Cl、SO42、SO32、HCO3、Na+、Mg2+、Fe3+,为了确定该溶液的组成,某同学取100mL上述溶液X,进行了如下实验,下列说法不正确的是

A. 气体A可能是CO2或SO2
B. 溶液X中一定存在SO42
C. 溶液X中一定不存在Fe3+和Mg2+,可能存在Na+
D. 向溶液A加入硝酸酸化的硝酸银溶液可能生成白色沉淀
【答案】C
【解析】
由实验流程可知,X与Ba(OH)2反应生成白色沉淀,则一定不含Fe3+,且白色沉淀A与足量盐酸反应,白色沉淀B一定为BaSO4,溶液中一定含有SO42-,气体A为CO2或SO2,溶液中可能含有SO32-或HCO3-两者中的一个或两种都存在,如果存在SO32-,SO32-、Mg2+相互促进水解不能共存,所以溶液中不存在Mg2+,如果不存在SO32-,溶液中可能含有在Mg2+,不确定是否含有Na+、Cl-,以此来解答.
A、白色沉淀A部分溶于酸,溶于酸的部分则可能是碳酸钡或亚硫酸钡,所以气体A可能是CO2或SO2,故A正确;
B、X与Ba(OH)2反应生成白色沉淀,且白色沉淀A与足量盐酸反应,白色沉淀B一定为BaSO4,溶液中一定含有SO42-,故B正确;
C、X与Ba(OH)2反应生成白色沉淀,则一定不含Fe3+,但溶液中可能含Mg2+ 、Na+,故C错误;
D、由上述分析可知溶液中不确定是否含有Cl-,因此向溶液A加入硝酸酸化的硝酸银溶液可能生成白色沉淀溶液AgCl,故D正确;
综上所述,本题正确答案为C。

【题目】在2 L密闭容器中,800 ℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
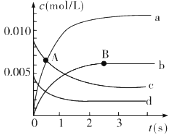
反应过程如图所示,其中只有3条曲线是正确的。请回答:
(1)A点处,v(正)____v(逆) (填“大于”“小于”或“等于”,下同),A点正反应速率_______B点正反应速率。
(2)图中表示NO2的变化的曲线是___。用O2表示从0~2 s内该反应的平均速率v=__。
(3)能说明该反应已经达到平衡状态的是________ (填字母)。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内的密度保持不变
(4)能使该反应的反应速率增大的是________(填字母)。
a.及时分离出NO2气体 b.适当升高温度
c.减小O2的浓度 d.选择高效的催化剂