题目内容
3.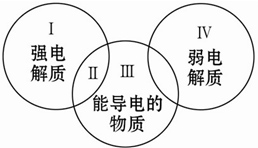 对下列物质:①镁 ②石墨 ③熔融氯化钠 ④盐酸 ⑤稀硫酸 ⑥氨水 ⑦白磷 ⑧硫酸钡 ⑨冰醋酸 ⑩二氧化碳,分类正确的是( )
对下列物质:①镁 ②石墨 ③熔融氯化钠 ④盐酸 ⑤稀硫酸 ⑥氨水 ⑦白磷 ⑧硫酸钡 ⑨冰醋酸 ⑩二氧化碳,分类正确的是( )| A. | Ⅰ包含的物质有③④⑤⑧ | B. | Ⅱ中包含的物质是③ | ||
| C. | Ⅲ中包含的物质是①②③⑤⑥⑧ | D. | Ⅳ中包含的物质是⑥⑨⑩ |
分析 电解质是指:在水溶液中或熔融状态下能够导电的化合物,完全电离的属于强电解质,如强酸、强碱与大部分盐;部分电离的属于弱电解质,如弱酸、弱碱和少部分盐;
单质,混合物既不是电解质也不是非电解质;能导电的物质含有自由移动的电子或阴阳离子,比如金属单质、石墨等,但不是电解质;根据定义即可解答.
解答 解:A、I为强电解质,④盐酸 和⑤稀硫酸属于混合物,不是化合物,故不是电解质,故A错误;
B、③熔融氯化钠既能导电,又是强电解质,故B正确;
C、金属单质①镁能导电,非金属单质 ②石墨能导电,③熔融氯化钠能导电,④盐酸和⑤稀硫酸能导电,⑥氨水也能导电,⑧硫酸钡无自由移动的离子,不能导电,故C错误;
D、⑥氨水是混合物,不是电解质,⑨冰醋酸为弱酸,属于弱电解质,⑩二氧化碳自身不能电离,属于非金点子,故D错误,
故选B.
点评 本题考查了电解质和非电解质的判断及能导电的物质,注意能导电的物质不一定是电解质,电解质不一定导电,为易错点.题目难度不大.

练习册系列答案
相关题目
11.下列方程式正确的是( )
| A. | 常温下,将铁片置于浓硝酸中:Fe+6HNO3(浓)═Fe(NO3)3+3NO2↑+3H2O | |
| B. | 向氯化铵的稀溶液中加入少量NaOH:NH4++OH-═NH3↑+H2O | |
| C. | 向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-═BaSO4↓ | |
| D. | 向浓硝酸中加入铜片:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
18.下列说法错误的是( )
| A. | 需要加热方能发生的反应不一定是吸热反应 | |
| B. | 放热的反应在常温下一定很容易发生 | |
| C. | 反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小 | |
| D. | 吸热反应在一定的条件下也能发生 |
15.下列根据元素周期表和元素周期律得出的推断中正确的是( )
| A. | 金属元素原子最外层电子数越少,该金属失电子能力越强 | |
| B. | 若存在简单阴离子R2-,则R一定位于ⅥA族 | |
| C. | aA2+、bB+、cC3-三种离子具有相同的电子层结构,则原子序数c>a>b | |
| D. | 铅位于周期表中金属和非金属的交界处,可作半导体材料 |
12.某有机物中有一个C6H5-,一个-CH2-,一个-C6H4-,一个-OH,则该有机物中能使FeCl3溶液显紫色结构有( )
| A. | 二种 | B. | 三种 | C. | 四种 | D. | 五种 |
13.下列物质中,既有离子键,又有共价键的是( )
| A. | H2O | B. | CaCl2 | C. | KOH | D. | Na2O2 |
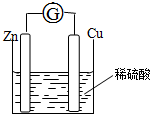 将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计,装置如图:
将锌片和铜片用导线相连浸入稀硫酸中组成原电池,两电极间连接一个电流计,装置如图: