题目内容
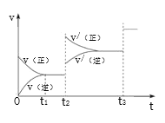
【题目】25℃时,用0.1mol·L-1的KOH溶液滴定10mL0.1mol·L-1的H2C2O4溶液,所得滴定曲线如图所示。忽略混合时溶液体积的变化,下列有关各点溶液中粒子浓度关系正确的是

A.a点溶液中:c(H+)=0.1mol·L-1+c(OH-)-c(H2C2O4)+c(C2O42-)
B.b点溶液中:c(K+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
C.c点溶液中:c(K+)<c(C2O42-)-c(H2C2O4)+0.1mol·L-1
D.d点溶液中:c(OH-)-c(H+)=c(H2C2O4)+c(HC2O4-)
【答案】AC
【解析】
A.根据物料守恒,a点溶液中有:c(H2C2O4)+c(C2O42-) +c(HC2O4-)=0.1mol·L-1,即c(C2O42-) +c(HC2O4-)=0.1mol·L-1- c(H2C2O4),电荷守恒有 c(H+)=2c(C2O42-) +c(HC2O4-)+c(OH-)= 0.1mol·L-1- c(H2C2O4) +c(C2O42-)+c(OH-),选项A正确;
B. b点时加入10mLKOH溶液,生成KHC2O4溶液,由图像可知,该溶液显酸性,所以HC2O4-的电离程度大于其水解程度,所以c(C2O42-)>c(H2C2O4),选项B错误;
C.c点时,溶液呈中性,c(H+)=c(OH-),结合电荷守恒得c(K+)=c(HC2O4-)+2 c(C2O42- ),溶液变稀,结合物料守恒有c(H2C2O4)+c(C2O42-) +c(HC2O4-)<0.1mol·L-1,则c(K+)=c(HC2O4-)+2 c(C2O42- )= c(H2C2O4)+c(C2O42-) +c(HC2O4-)+ c(C2O42-)- c(H2C2O4),故有c(K+)<c(C2O42-)-c(H2C2O4)+0.1mol·L-1,选项C正确;
D. d点时加入20mLKOH溶液,生成K2C2O4溶液,存在质子守恒:c(OH-)=c(H+)+2c(H2C2O4)+c(HC2O4-),故有c(OH-)-c(H+)=2c(H2C2O4)+c(HC2O4-),选项D错误;
答案选AC。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】25 ℃时有关物质的颜色和溶度积(Ksp)如下表:
物质 | AgCl | AgBr | AgI | Ag2S |
颜色 | 白 | 淡黄 | 黄 | 黑 |
Ksp | 1.8×10-10 | 7.7×10-13 | 1.5×10-16 | 1.8×10-50 |
下列叙述中不正确的是( )
A.向AgCl的白色悬浊液中加入0.1 mol/L KI溶液,有黄色沉淀产生
B.25 ℃时,利用表中的溶度积(Ksp),可以计算AgCl、AgBr、AgI、Ag2S饱和水溶液中Ag+的浓度
C.25 ℃,AgCl固体分别在等物质的量浓度NaCl、CaCl2溶液中溶解达到平衡,两溶液中,c(Ag+)和溶度积均相同
D.在5 mL 1.8×10-6 mol/L NaCl溶液中,加入1滴(20滴约为1 mL)1×10-3 mol/L AgNO3溶液,不能产生白色沉淀
【题目】钒及其化合物在工业上有许多用途。某钒精矿的主要成分及质量分数如下表:
物质 | V2O5 | V2O3 | K2O | SiO2 | Fe2O3 | Al2O3 |
质量分数% | 0.81 | 1.70 | 2.11 | 63.91 | 5.86 | 12.51 |
一种从该钒精矿中提取五氧化二钒的流程如下:

回答下列问题:
(1)“酸浸、氧化”时,V2O3转化为VO2+,反应的离子方程式为____________________________________;若用浓盐酸代替硫酸,V2O5转化为VO2+,同时生成有毒的黄绿色气体,反应的化学方程式为__________________。
(2)萃取剂对四价钒具有高选择性,且萃取Fe3+而不萃取Fe2+,所以萃取前可用____________(填名称,下同)对浸出液进行“还原”处理。为检验“还原”后的滤液中是否含有Fe3+,可选用的化学试剂是____________________。
(3)“溶剂萃取与反萃取”可表示为:VO2+ + (HR2PO4)2(O)![]() VO(R2PO4)2(O)+ 2H+。其中(HR2PO4)2(O)为萃取剂,为了提高VO2+的产率,反萃取剂应该呈 __________性(填“酸”“碱”或“中”)。
VO(R2PO4)2(O)+ 2H+。其中(HR2PO4)2(O)为萃取剂,为了提高VO2+的产率,反萃取剂应该呈 __________性(填“酸”“碱”或“中”)。
(4)“氧化”中,欲使3molVO2+变为VO2+,则需要氧化剂NaClO3至少为____________mol。
(5)单质钒可用于制造特种合金钢。以五氧化二钒和金属钙为原料在高温条件下可制备单质钒,表示制备过程的化学方程式为________________________________________。