题目内容
11.将1mol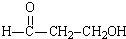 加入到足量的酸性KMnO4溶液中,充分反应后生成丙二酸,锰元素在生成物中为+2价,则消耗KMnO4的物质的量是( )
加入到足量的酸性KMnO4溶液中,充分反应后生成丙二酸,锰元素在生成物中为+2价,则消耗KMnO4的物质的量是( )| A. | 0.4mol | B. | 0.6mol | C. | 0.8mol | D. | 1.2mol |
分析 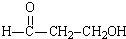 转化为HOOCCH2COOH,反应中碳元素的化合价从-$\frac{2}{3}$升高到+$\frac{4}{3}$,KMnO4转化为Mn2+,Mn元素降低5价,根据电子守恒计算.
转化为HOOCCH2COOH,反应中碳元素的化合价从-$\frac{2}{3}$升高到+$\frac{4}{3}$,KMnO4转化为Mn2+,Mn元素降低5价,根据电子守恒计算.
解答 解: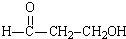 转化为HOOCCH2COOH,反应中碳元素的化合价从-$\frac{2}{3}$升高到+$\frac{4}{3}$,KMnO4转化为Mn2+,Mn元素降低5价,
转化为HOOCCH2COOH,反应中碳元素的化合价从-$\frac{2}{3}$升高到+$\frac{4}{3}$,KMnO4转化为Mn2+,Mn元素降低5价,
设消耗的KMnO4的物质的量为nmol,
则1mol×($\frac{4}{3}$+$\frac{2}{3}$)×3=5×n,
解得n=1.2mol.
故选D.
点评 本题考查了氧化还原反应的计算,注意根据电子守恒计算,题目难度不大,注意根据在化合物中正负化合价代数和为零计算有机物中C元素的化合价.

练习册系列答案
相关题目
1.某粒子用符号AZMn+表示,下列关于该粒子的叙述中,正确的是( )
| A. | 所含质子数为(A-n) | B. | 所含中子数为(A-Z) | ||
| C. | 所含电子数为(Z+n) | D. | 中子数-电子数=A-2Z-n |
2. 空气中CO2含量偏高会产生温室效应,也会对人体健康造成影响;CO2的用途广泛,合理使用则可缓解由CO2累积所产生的温室效应,实现CO2的良性循环.
空气中CO2含量偏高会产生温室效应,也会对人体健康造成影响;CO2的用途广泛,合理使用则可缓解由CO2累积所产生的温室效应,实现CO2的良性循环.
(1)一定条件下CO2可制得Na2CO3、NaHCO3等.
①等物质的量浓度的Na2CO3、NaHCO3溶液,碱性前者>后者(填“>”“<”或“=”).
②有下列五种物质的量浓度均为0.1mol/L的电解质溶液,将其稀释相同倍数时,pH变化最大的是E(填字母编号).
A.Na2CO3B.NaHCO3 C.NaAlO2 D.CH3COONa E.NaOH
(2)已知反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H=a kJ/mol,测得在不同温度下,
该反应的平衡常数K随温度的变化如下:
上述反应中a>0(填“>”、“<”或“=”);在2L密闭容器中300℃下进行反应,若Fe和CO2的起始量均为4mol,当达到平衡时CO2的转化率为75%.
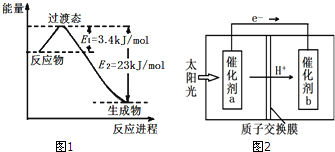
(3)目前工业上可以用CO2和H2在230℃、催化剂条件下反应生成甲醇蒸汽和水蒸气.图1为恒压容器中0.5mol CO2和1.5mol H2反应转化率达80%时的能量变化示意图.则该反应的热化学方程式为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49 kJ/mol.
(4)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.图2是制备HCOOH的示意图,根据要求回答问题:
①催化剂b表面的电极反应式为CO2+2e-+2H+=HCOOH.
②经测定,若每分钟通过质子交换膜的H+的物质的量为40mol,则每小时可产生O219.2Kg.
 空气中CO2含量偏高会产生温室效应,也会对人体健康造成影响;CO2的用途广泛,合理使用则可缓解由CO2累积所产生的温室效应,实现CO2的良性循环.
空气中CO2含量偏高会产生温室效应,也会对人体健康造成影响;CO2的用途广泛,合理使用则可缓解由CO2累积所产生的温室效应,实现CO2的良性循环.(1)一定条件下CO2可制得Na2CO3、NaHCO3等.
①等物质的量浓度的Na2CO3、NaHCO3溶液,碱性前者>后者(填“>”“<”或“=”).
②有下列五种物质的量浓度均为0.1mol/L的电解质溶液,将其稀释相同倍数时,pH变化最大的是E(填字母编号).
A.Na2CO3B.NaHCO3 C.NaAlO2 D.CH3COONa E.NaOH
(2)已知反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H=a kJ/mol,测得在不同温度下,
该反应的平衡常数K随温度的变化如下:
| 温度(℃) | 300 | 500 | 700 |
| K | 3.00 | 3.47 | 4.40 |
(3)目前工业上可以用CO2和H2在230℃、催化剂条件下反应生成甲醇蒸汽和水蒸气.图1为恒压容器中0.5mol CO2和1.5mol H2反应转化率达80%时的能量变化示意图.则该反应的热化学方程式为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49 kJ/mol.
(4)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.图2是制备HCOOH的示意图,根据要求回答问题:
①催化剂b表面的电极反应式为CO2+2e-+2H+=HCOOH.
②经测定,若每分钟通过质子交换膜的H+的物质的量为40mol,则每小时可产生O219.2Kg.
19.下表中,对陈述I、II的正确性及两者间有无因果关系的判断都正确的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 用锌和足量稀硫酸制取氢气时加入硫酸铜溶液 | 可以加快制取氢气的速度 | Ⅰ对、Ⅱ对、无 |
| B | 用Mg-Al-NaOH构成原电池 | Mg更活泼作负极 | Ⅰ对、Ⅱ对、无 |
| C | 石墨常用做电解池的电极 | 石墨的化学性质稳定且导电性好 | Ⅰ对、Ⅱ对、有 |
| D | MgCl2是离子化合物 | 电解MgCl2的饱和溶液制取金属镁 | Ⅰ对、Ⅱ对、有 |
| A. | A | B. | B | C. | C | D. | D |
16.下列说法中正确的是( )
| A. | 摩尔就是物质的量 | B. | 摩尔是物质质量的单位 | ||
| C. | 氢气的摩尔质量是2g/mol | D. | 气体摩尔体积的单位为升 |
3.设NA是阿伏加德罗常数的数值.下列说法不正确的是( )
| A. | 7.8g Na2O2中含有的阴离子数目为0.1NA | |
| B. | 常温下,34gH2O2中H-O键数目为2NA | |
| C. | 1.00mol NaCl晶体中含有NA个NaCl分子 | |
| D. | 在20g D216O中含有10 NA个电子 |
20.可以证明可逆反应N2+3H2?2NH3已达到平衡状态的是( )
①一个N≡N键断裂的同时,有3个H-H键断裂
②一个N≡N键断裂的同时,有6个N-H键断裂
③其它条件不变时,混合气体平均相对分子质量不再改变
④保持其它条件不变时,体系压强不再改变⑤NH3%、N2%、H2%都不再改变.
①一个N≡N键断裂的同时,有3个H-H键断裂
②一个N≡N键断裂的同时,有6个N-H键断裂
③其它条件不变时,混合气体平均相对分子质量不再改变
④保持其它条件不变时,体系压强不再改变⑤NH3%、N2%、H2%都不再改变.
| A. | 全部 | B. | 只有①③④⑤ | C. | ②③④⑤ | D. | 只有①③⑤ |
1.下列物质中,能在空气中稳定保存的是( )
| A. | NaOH固体 | B. | 稀H2SO4 | C. | Na2SO3晶体 | D. | 水玻璃 |