题目内容
8.下列化学用语的表达方式正确的是( )①乙酸乙酯的结构简式:CH3CH2COOCH2CH3
②CO2分子的结构式:O=C=O
③乙烯的实验式:C2H4
④S原子的结构示意图:
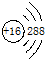
⑤葡萄糖结构简式:C6H12O6
⑥CH4Si的结构式
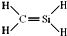
| A. | 只有②⑥ | B. | 只有③④ | C. | 只有②③⑥ | D. | 只有①②⑥ |
分析 ①乙酸乙酯是乙酸和乙醇反应生成,含有四个碳原子;
②由最外层电子及形成8电子稳定结构可知,存在C=O;
③实验式中原子个数为最简比;
④硫原子核外存在16个电子核内有16个质子,写微粒结构示意图;
⑤葡萄糖为多羟基醛,含有5个羟基一个醛基;
⑥依据乙烯结构推断得到结构式.
解答 解:①乙酸乙酯的结构简式:CH3COOCH2CH3,故①错误;
②由最外层电子及形成8电子稳定结构可知,存在C=O,则CO2分子的结构式O=C=O,故②正确;
③实验式中原子个数为最简比,则乙烯的实验式为CH2,故③错误;
④硫原子最外层6个电子,硫原子核外存在16个电子核内有16个质子,其微粒结构示意图为: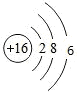 ,故④错误;
,故④错误;
⑤葡萄糖分子中含有6个碳原子、12个氢原子、6个氧原子,分子式为:C6H12O6,6个碳原子成链状,末端碳原子上链有1个醛基,其余每个碳原子上各连接一个羟基,结构简式为:CH2OHCHOHCHOHCHOHCHOHCHO,故⑤错误;
⑥依据乙烯结构推断得到结构式,CH4Si的结构式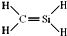 ,故⑥正确;
,故⑥正确;
故选A.
点评 本题考查化学用语,涉及结构式、实验式、结构简式、结构示意图等,综合性较强,注重基础知识的考查,把握化学用语的区别及规范应用,题目难度不大.

练习册系列答案
相关题目
18.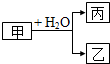 甲、乙、丙是常见的三种物质,它们之间有如图所示的转化关系.根据要求回答问题:
甲、乙、丙是常见的三种物质,它们之间有如图所示的转化关系.根据要求回答问题:
Ⅰ.已知:甲是常见单质,丙为氢气.
(1)若乙为氧化物且有磁性,则乙发生铝热反应的化学方程式为8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe.
(2)若甲为碳,则产物乙、丙可合成甲醇.
①已知:CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.0kJ•mol-1
CH4(g)+H2O(g)?CH3OH(g)+H2(g)△H=+77.0kJ•mol-1
写出气体乙与气体丙反应生成CH3OH(g)的热化学方程式:CO(g)+2H2(g)=CH3OH(g)△H=-129.0kJ•mol-1.
②乙和丙合成甲醇的反应在不同温度下的化学平衡常数(K)如下表.则T1< T2(填“>”“<”、“=”).
③乙可做某碱性燃料电池的燃料,该电池的负极反应式为CO-2e-+4OH-=CO32-+2H2O.
Ⅱ.已知:甲是由两种短周期元素组成的化合物,丙的水溶液显碱性.
(3)若构成甲的阴、阳离子个数比为2:3,丙是气体.则构成甲的阴、阳离子半径大小关系为N3->Mg2+(用具体的微粒表示).
(4)若乙是O2,则甲的一种重要用途是供氧剂或漂白剂;产物丙与Cl2按2:1(物质的量)反应得到丁溶液,丁溶液中阴离子浓度从大到小的顺序是c(Cl-)>c(ClO-)>C(OH-).
 甲、乙、丙是常见的三种物质,它们之间有如图所示的转化关系.根据要求回答问题:
甲、乙、丙是常见的三种物质,它们之间有如图所示的转化关系.根据要求回答问题:Ⅰ.已知:甲是常见单质,丙为氢气.
(1)若乙为氧化物且有磁性,则乙发生铝热反应的化学方程式为8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe.
(2)若甲为碳,则产物乙、丙可合成甲醇.
①已知:CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.0kJ•mol-1
CH4(g)+H2O(g)?CH3OH(g)+H2(g)△H=+77.0kJ•mol-1
写出气体乙与气体丙反应生成CH3OH(g)的热化学方程式:CO(g)+2H2(g)=CH3OH(g)△H=-129.0kJ•mol-1.
②乙和丙合成甲醇的反应在不同温度下的化学平衡常数(K)如下表.则T1< T2(填“>”“<”、“=”).
| 温度/℃ | T1 | T2 |
| K | 2.041 | 0.012 |
Ⅱ.已知:甲是由两种短周期元素组成的化合物,丙的水溶液显碱性.
(3)若构成甲的阴、阳离子个数比为2:3,丙是气体.则构成甲的阴、阳离子半径大小关系为N3->Mg2+(用具体的微粒表示).
(4)若乙是O2,则甲的一种重要用途是供氧剂或漂白剂;产物丙与Cl2按2:1(物质的量)反应得到丁溶液,丁溶液中阴离子浓度从大到小的顺序是c(Cl-)>c(ClO-)>C(OH-).
19.下列实验操作中,正确的是( )
| A. | 用剩的药品不要乱丢,要放回原试剂瓶里 | |
| B. | 给试管里的液体加热,液体的体积一般不超过试管容积的$\frac{1}{3}$ | |
| C. | 试管和烧杯都可以直接在火焰上加热 | |
| D. | 加热后的蒸发皿,要用坩埚钳夹取 |
16.影响化学反应速率的因素很多,下列措施中能减慢化学反应速率的是( )
| A. | 用铁粉代替铁钉与稀盐酸反应 | |
| B. | 将食物由常温保存改为在冰箱中保存 | |
| C. | 加入MnO2粉末做H2O2分解反应的催化剂 | |
| D. | 用 3 mol/L 的盐酸代替 1 mol/L 的盐酸与锌粒反应 |
3.下列关于化石燃料的说法错误的是( )
| A. | 石油中含有C5~C11的烷烃,可以通过石油的分馏得到汽油 | |
| B. | 含C18以上烷烃的重油经过催化裂化可以得到汽油 | |
| C. | 煤是由有机化合物和无机物组成的复杂的混合物 | |
| D. | 煤中含有苯和甲苯,可以用分馏的方法把它们从煤中分离出来 |
13.在一定条件下,16g A恰好能跟20g B完全反应,生成C和4.5g D;若在相同条件下,将8g A和15g B反应时,则生成D和0.125mol的C,则物质C的摩尔质量是( )
| A. | 252 g•mol-1 | B. | 168 g•mol-1 | C. | 126 g•mol-1 | D. | 36 g•mol-1 |
20.下列气体不能用碱石灰干燥的是( )
| A. | H2 | B. | Cl2 | C. | NH3 | D. | CO |
18.下列四个反应中,有一个与另外三个的反应类型不同,该反应是( )
| A. | 溴乙烷与NaOH水溶液共热 | |
| B. | 油脂与NaOH水溶液共热 | |
| C. | 甲酸钠与NaOH、Cu(OH)2悬浊液混合共热 | |
| D. | 2,2-二甲基-1-丙醇与浓硫酸共热 |