��Ŀ����
����Ŀ��ʵ������Ҫ����0.50 mol��L��1NaCl��Һ480 mL�������в������������ʵ������֣���ʹ��������������
(1)ѡ����������ɱ�ʵ��������������У�������ƽ(��ȷ��0.1 g)��ҩ�ס��ձ�����������________��________�Լ�����������Ƭ��ֽ��
(2)���㡣���Ƹ���Һ��ȡNaCl����________g��
(3)������
����ƽ��ƽ֮��Ӧ����ƽ���������ij��λ�ã�������ͼ����һ�����߱���������Ե������λ�ã�

�ڳ���������NaCl����Ӧ������ƽ��________(����̡������̡�)��
�۳�����ϣ���ҩƷ�����ձ��С�
(4)�ܽ⡢��ȴ���ò�ʵ������Ҫʹ�ò�������Ŀ����_________________��
(5)ת�ơ�ϴ�ӡ���ת��ʱӦʹ��________��������Ҫϴ���ձ�2��3����Ϊ��_____________��
(6)���ݣ�ҡ�ȡ�
(7)����õ���Һ����һ��ʱ�����ָ�����Լ�ƿ�������ñ�ǩ��ע�����Ƶ�ʱ�䡢��Һ���Ƽ�Ũ�ȡ�
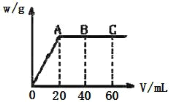
(8)�����ƹ����У�ijѧ���۲춨��ʱҺ�������ͼ��ʾ��������Һ��Ũ�Ȼ�________(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��

���𰸡�500 mL����ƿ��ͷ�ι�14.6���̽��裬����NaCl�ܽⲣ������֤����ȫ��ת��������ƿ��ƫ��
��������
���⣨1������һ�����ʵ���Ũ�ȵ���Һ��Ҫ�õ�������ƽ����Ͳ�����ձ���������������ƿ����ͷ�ιܣ�����ƿ�Ĺ����100mL��250mL��500mL��1000mL�������Ҫ500mL����ƿ�ͽ�ͷ�ιܣ�
��2����Ҫ�Ȼ��Ƶ�����Ϊm��NaCl����500��10��3��0.5��58.5g=14.6g��
��3������������ƽ��ʹ����������������֪NaCl���������ƽ�����̣�
��4���ܽ�ʹ�ò��������н��裬�����Ȼ��Ƶ��ܽ⣻
��5��ת��ʱӦʹ�ò�������������ֹ��Һ�������棬�������Ũ�Ȳ�����Ҫϴ���ձ��Ͳ�����2��3�Σ�Ϊ�˱�֤����ȫ��ת��������ƿ�У�
��7������õ���Һ����һ��ʱ�����ָ�����Լ�ƿ�������ñ�ǩ��ע�����Ƶ�ʱ�䡢Ũ�ȡ����ƣ�
��8�����Ӷ�����������Һ����������ʵ����ʵ������䣬���Ũ�Ƚ�ƫ�͡�

����Ŀ���±���25��ʱ��������ĵ���ƽ�ⳣ����
��ѧʽ | HA��A����ij������� | HNO2 | H2CO3 |
Ka | Ka��4.9��10��10 | Ka��4.6��10��4 | Ka1��4.1��10��7 Ka2��5.6��10��11 |
�ش��������⣺
��1�������ӷ���ʽ��ʾNaNO2��Һ�ʼ��Ե�ԭ��____________________��
��2��A����CO32����HCO3����ˮ�н��H+�������ɴ�С��˳��Ϊ____________��
��3��25��ʱ�������ʵ���Ũ�ȵ�HA��NaA�Ļ����Һ�ʼ��ԣ���û����Һ�и�����Ũ�ȴ�С��ϵΪ________________�����ͻ����Һ�ʼ��Ե�ԭ��_________________________________��
��4��д��NaA��Һ��ͨ����CO2�����ӷ���ʽ_______________________________________��
��5��ijͬѧ��Na2CO3��NaHCO3��Һ��������ͼ��ʾʵ����

�� ��ַ�Ӧ��a�Թ��д������ڵ�������_______________________________________��
�� �����ӷ���ʽ��ʾb�Թ��з����ķ�Ӧ_______________________________________��