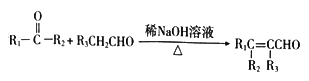
题目内容
【题目】将一定质量的Na、Na2O、Na2O2的混合物与足量水反应,在标准状况下得到6.72L 混合气体,将混合气体用电火花引燃,恰好完全反应,则Na与Na2O2的物质的量之比为
A. l : 2 B. 1 : 1 C. 2 : 1 D. 3 : 1
【答案】C
【解析】钠与水、过氧化钠与水、氢气与氧气的反应方程式如下:2Na+2H2O=2NaOH+H2↑ 钠与氢气的关系式为:2Na~H2,2Na2O2+2H2O=4NaOH+O2↑ 过氧化钠与氧气的关系式为:2Na2O2~O2,2H2+O2![]() 2H2O 氢气和氧气的关系式为:2H2~O2,将该混合气体通过放电,恰好完全反应,说明氢气和氧气反应的物质的量之比恰好等于它们反应的计量数之比,即氢气和氧气的物质的量之比为2∶1,通过钠与氢气、过氧化钠与氧气、氢气与氧气的关系式可得钠与过氧化钠的关系式为:4Na-2H2-O2-2Na2O2,所以钠与过氧化钠的物质的量之比为4∶2=2∶1,故答案为C。
2H2O 氢气和氧气的关系式为:2H2~O2,将该混合气体通过放电,恰好完全反应,说明氢气和氧气反应的物质的量之比恰好等于它们反应的计量数之比,即氢气和氧气的物质的量之比为2∶1,通过钠与氢气、过氧化钠与氧气、氢气与氧气的关系式可得钠与过氧化钠的关系式为:4Na-2H2-O2-2Na2O2,所以钠与过氧化钠的物质的量之比为4∶2=2∶1,故答案为C。

 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案【题目】短周期元素甲~戊在元素周期表中的相对位置如下表所示,下列判断正确的是( )
甲 | 乙 | |
丙 | 丁 | 戊 |
A. 原子半径:甲>乙
B. 原子核外电子层数:乙<丁
C. 原子最外层电子数:丙>丁>戊
D. 元素的最高价氧化物对应水化物的碱性:丙<戊
【题目】工业上用含锰废料(主要成分MnO2,含有少量Fe2O3、Al2O3、CuO、CaO等)与烟气脱硫进行联合处理并制备MnSO4的流程如下:

已知:25℃时,部分氢氧化物的溶度积常数(Ksp)如下表所示。
氢氧化物 | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mn(OH)2 |
Ksp | 1.0×10-33 | 4.0×10-38 | 2.0×10-20 | 4.0×10-14 |
请回答:
(1)沉淀1的化学式为__________________。
(2)(NH4)2S的电子式为________________;“净化”时,加入(NH4)2S的作用为___________________。
(3)“酸化、还原”中,发生的所有氧化还原反应的离子方程式为__________________。
(4)已知:滤液3中除MnSO4外,还含有少量(NH4)2SO4。(NH4)2SO4、MnSO4的溶解度曲线如下图所示。
据此判断,操作“I”应为蒸发浓缩、____________、洗涤、干燥。

(5)工业上可用电解酸性MnSO4溶液的方法制备MnO2,其阳极反应式为________________。
(6)25.35 g MnSO4·H2O样品受热分解过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
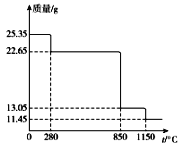
①300℃时,所得固体的化学式为______________________。
②1150℃时,反应的化学方程式为___________________。