题目内容
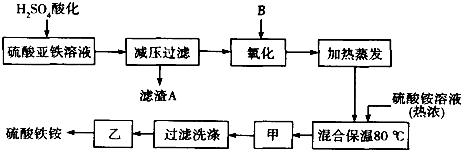
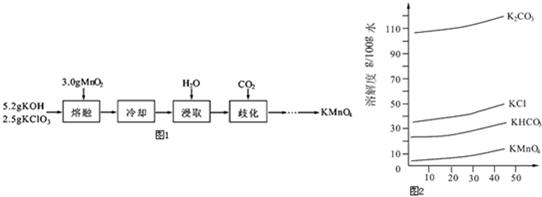
13.实验室用MnO2、KOH及KClO3为原料制取高锰酸钾的实验流程如图1:(1)熔融时需用铁坩埚和铁制搅拌棒而不能用玻璃仪器,其原因是在高温下,瓷坩埚可以和KOH发生反应SiO2+2KOH═K2SiO3+H2O,腐蚀瓷坩埚.
(2)熔融时,MnO2转化为K2MnO4,KClO3转化为KCl,其反应的化学方程式为KClO3+3MnO2+6KOH$\frac{\underline{\;高温\;}}{\;}$ KCl+3K2MnO4+3H2O.
(3)几种物质的溶解度曲线如图2所示.
①歧化时,通入CO2至pH为10~11,K2MnO4绿色溶液转化为KMnO4和MnO2.其反应的离子方程式为3MnO42-+2CO2=2MnO4-+MnO2↓+2CO32-.
②歧化时不能通入过量CO2的原因是二氧化碳过量会生成溶解度比K2CO3小得多的KHCO3,可能与KMnO4同时析出.
③通入CO2后,用玻璃棒蘸取溶液点于滤纸上,观察到滤纸上有紫红色,证明歧化反应已发生.
④歧化后得到KMnO4晶体的操作依次为过滤、加热浓缩、趁热过滤及干燥.
(4)在此实验流程中可循环使用的物质的化学式为MnO2.
分析 (1)从瓷坩埚原料含有SiO2,高温下与KOH发生反应进行分析;
(2)由题意可知,KOH、KClO3、MnO2共熔制得绿色K2MnO4,根据氧化还原反应可知,还生成KCl,由元素守恒可知,还会生成H2O;
MnO2存在,高温下KClO3可能发生分解反应生成氯化钾与氧气;
(3)①依据氧化还原反应原理书写离子反应方程式即可;
②由溶解度曲线可知,KHCO3的溶解度较小,过量的二氧化碳会生成碳酸氢钾,与高锰酸钾同时析出,据此解答即可;
③高锰酸钾为紫红色溶液,据此解答即可;
④依据从溶液中得到固体的方法回答即可;
(4)熔融过程中加入二氧化锰,歧化反应中生成二氧化锰,据此解答.
解答 解:(1)瓷坩埚原料含有SiO2,在高温下,瓷坩埚可以和KOH发生反应SiO2+2KOH═K2SiO3+H2O,腐蚀瓷坩埚,故不能使用瓷坩埚,而使用铁坩埚,
故答案为:在高温下,瓷坩埚可以和KOH发生反应SiO2+2KOH═K2SiO3+H2O,腐蚀瓷坩埚;
(2)由题意可知,KOH、KClO3、MnO2共熔制得绿色K2MnO4,根据氧化还原反应可知,还生成KCl,由元素守恒可知,还会生成H2O,反应方程式为KClO3+3MnO2+6KOH $\frac{\underline{\;高温\;}}{\;}$KCl+3K2MnO4+3H2O,故答案为:KClO3+3MnO2+6KOH $\frac{\underline{\;高温\;}}{\;}$KCl+3K2MnO4+3H2O;
(3)①此反应中锰酸钾既作氧化剂又作氧化剂,发生歧化反应,+6价的Mn部分升高为+7价,部分降低为+4价,碱性溶液中二氧化碳变为碳酸根,故方程式为:3MnO42-+2CO2=2MnO4-+MnO2↓+2CO32-,故答案为:3MnO42-+2CO2=2MnO4-+MnO2↓+2CO32-;
②由溶解度曲线可知,KHCO3的溶解度较小,过量的二氧化碳会生成碳酸氢钾,与高锰酸钾同时析出,对高锰酸钾的制取造成干扰,
故答案为:二氧化碳过量会生成溶解度比K2CO3小得多的KHCO3,可能与KMnO4同时析出;
③若有高锰酸钾生成,溶液应显示紫红色,故取少许溶液于滤纸上,若观察到紫色,说明有高锰酸钾产生,
故答案为:滤纸上有紫红色;
④从溶液中得到固体,需经过过滤、加热浓缩、趁热过滤、干燥等操作,
故答案为:加热浓缩;趁热过滤;
(4)从整个制取流程可以看出熔融过程中加入二氧化锰固体,在通入二氧化碳的歧化反应中又生成,据此得出二氧化锰固体可以循环利用,
故答案为:MnO2.
点评 本题考查学生对工艺流程的理解、阅读获取信息能力、物质推断、氧化还原反应、工艺条件的控制等,难度中等,是对所学知识的综合运用与能力的考查,需要学生具备扎实的基础知识与综合运用知识、信息进行解决问题的能力.

| A. | 0.3 mol HNO3 | B. | 3.01×10 23个 H2O分子 | ||
| C. | 3.4 g H2S | D. | 8.96L NH3(标准状况下) |
 在一定温度下,向2L体积固定的密闭容器中加入1molHI,2HI(g)═H2(g)+I2(g)△H>0,H2的物质的量随时间的变化如图示,下列说法正确的是( )
在一定温度下,向2L体积固定的密闭容器中加入1molHI,2HI(g)═H2(g)+I2(g)△H>0,H2的物质的量随时间的变化如图示,下列说法正确的是( )| A. | 该温度下,反应的平衡常数是$\frac{1}{8}$ | |
| B. | 0~2min内的HI的平均反应速率为0.05mol•L-1•min-1 | |
| C. | 恒压下向该体系中加入N2,平衡不移动,反应速率不变 | |
| D. | 升高温度,平衡向正反应方向移动,只有正反应速率加快 |
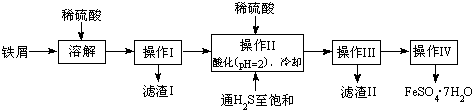
查询资料,得有关物质的数据如表:
| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
(2)操作II中,通入硫化氢至饱和的目的是:①除去溶液中的Sn2+离子;②防止Fe2+被氧化;③在溶液中用硫酸酸化至pH=2的目的是防止Fe2+离子生成沉淀.
(3)操作IV的顺序依次为蒸发浓缩、冷却结晶、过滤洗涤.
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;②降低洗涤过程中FeSO4•7H2O的损耗.
(5)已知常温下,Ksp[Fe(OH)2]=1.64×10-14,则求得反应:Fe2++2H2O?Fe(OH)2+2H+的平衡常数为:0.6×10-14(保留1位小数)
(6)测定绿矾产品中Fe2+含量的方法是:a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.计算上述样品中FeSO4•7H2O的质量分数为97.5%.(保留3位小数)
| A. | 以B表示的平均反应速率为v(B)=0.13mol•L-1•min-1 | |
| B. | 4min时,A的物质的量为0.75mol | |
| C. | 该反应方程式中,x=2 | |
| D. | 4min时,A的转化率为60% |
 如图表示的是A、B、C三种溶液两两混合发生反应的实验现象,符合该实验现象的A、B、C三种溶液依次是( )
如图表示的是A、B、C三种溶液两两混合发生反应的实验现象,符合该实验现象的A、B、C三种溶液依次是( )| A. | 盐酸、碳酸钠溶液、氢氧化钠溶液 | |
| B. | 氯化钠溶液、澄清石灰水、氢氧化钠溶液 | |
| C. | 盐酸、碳酸钠溶液、澄清石灰水 | |
| D. | 氢氧化钙溶液、盐酸、硫酸钠溶液 |
| 醋酸浓度/mol•L-1 | 0.001 0 | 0.010 0 | 0.020 0 | 0.100 0 | 0.200 0 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
(1)写出醋酸的电离方程式:CH3COOH?CH3COO-+H+.
(2)醋酸溶液中存在的微粒有H2O、CH3COOH、CH3COO-、H+、OH-.
(3)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是当醋酸浓度为0.001mol/L时,溶液中的氢离子浓度小于0.001mol/L.
(4)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度(选填“增大”“减小”或“不变”)增大.
(5)常温常压下,在 pH=5的稀醋酸溶液中,c(CH3COO-)=(10-5-10-9)mol/L (精确值,用表达式表示).
(6)下列方法中,可以使0.10mol•L-1CH3COOH溶液中CH3COOH电离程度增大的是de.
a.加入少量0.10mol•L-1的稀盐酸 b.加入少量冰醋酸
c.加入少量氯化钠固体 d.加热CH3COOH溶液
e.加入Zn粒 f.加入少量0.10mol•L-1的CH3COONa溶液.