题目内容
【题目】构成原电池的条件
(1)
(2)
(3)
(4) .
【答案】
(1)有两个活泼性不同的电极
(2)将电极插入电解质溶液中
(3)两电极间构成闭合回路
(4)能自发的进行氧化还原反应
【解析】解:原电池的构成条件是:1、有两个活泼性不同的电极,2、将电极插入电解质溶液中,3、两电极间构成闭合回路,4、能自发的进行氧化还原反应;原电池中正极上发生还原反应,负极上发生氧化反应,所以答案是:(1)有两个活泼性不同的电极;(2)将电极插入电解质溶液中;(3)两电极间构成闭合回路;(4)能自发的进行氧化还原反应.

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案【题目】甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)已知:CH3OH(g)=HCHO(g)+H2(g) ΔH=+84 kJ·mol-1
2H2(g)+O2(g)===2H2O(g) ΔH=-484 kJ·mol-1
工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:___。
(2)工业上可用如下方法合成甲醇,化学方程式为CO(g)+2H2(g)![]() CH3OH(g),已知某些化学键的键能数据如下表:
CH3OH(g),已知某些化学键的键能数据如下表:
化学键 | C—C | C—H | H—H | C—O | C≡O | O—H |
键能/ kJ·mol-1 | 348 | 413 | 436 | 358 | x | 463 |
请回答下列问题
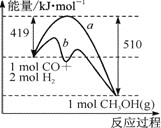
①该反应的ΔS____(填“>”或“<”)0。右图中曲线a到曲线b的措施是_______。
②已知CO中的C与O之间为三键,其键能为xkJ·mol-1,则x=____。
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。①该电池负极的电极反应式为__。
②若以该电池为电源,用石墨作电极电解200 mL含有如下离子的溶液。
离子 | Cu2+ | H+ | Cl | SO42- |
c/mol·L-1 | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件下)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为____。
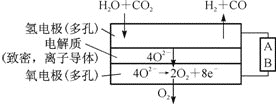
(4)电解水蒸气和CO2产生合成气(H2+CO)。较高温度下(700~1 000℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2,O2穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2。由上图可知A为直流电源的____(填“正极”或“负极”),请写出以H2O为原料生成H2的电极反应式:_______。