题目内容
已知在Na2HPO4溶于水后,它的水解程度远大于电离程度。对于平衡: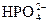 +H2O
+H2O H3O++
H3O++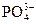 ,欲使溶液中c(
,欲使溶液中c(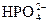 )、c(H3O+)、c(
)、c(H3O+)、c(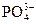 )均下降,可采用的方法是()
)均下降,可采用的方法是()
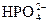 +H2O
+H2O H3O++
H3O++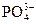 ,欲使溶液中c(
,欲使溶液中c(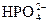 )、c(H3O+)、c(
)、c(H3O+)、c(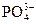 )均下降,可采用的方法是()
)均下降,可采用的方法是()| A.加少量水 | B.加热 |
| C.加消石灰 | D.加AgNO3 |
C
本题考查了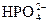 在水中的两个平衡:
在水中的两个平衡: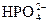 的电离:
的电离:
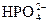 +H2O
+H2O H3O++
H3O++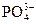 ,
,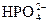 的水解:
的水解: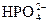 +H2O
+H2O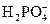 +OH-。题目中给出了电离方程式,误导答题者忽略前面给出的“水解程度大于电离程度”的已知条件,而误选A。加水稀释后,
+OH-。题目中给出了电离方程式,误导答题者忽略前面给出的“水解程度大于电离程度”的已知条件,而误选A。加水稀释后,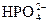 、
、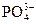 都减小,忽略了水解为主,溶液呈碱性,稀释时c(OH-)减小、c(H+)=
都减小,忽略了水解为主,溶液呈碱性,稀释时c(OH-)减小、c(H+)=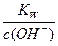 增大这一点。
增大这一点。
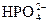 在水中的两个平衡:
在水中的两个平衡: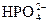 的电离:
的电离: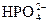 +H2O
+H2O H3O++
H3O++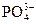 ,
,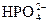 的水解:
的水解: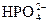 +H2O
+H2O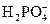 +OH-。题目中给出了电离方程式,误导答题者忽略前面给出的“水解程度大于电离程度”的已知条件,而误选A。加水稀释后,
+OH-。题目中给出了电离方程式,误导答题者忽略前面给出的“水解程度大于电离程度”的已知条件,而误选A。加水稀释后,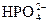 、
、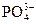 都减小,忽略了水解为主,溶液呈碱性,稀释时c(OH-)减小、c(H+)=
都减小,忽略了水解为主,溶液呈碱性,稀释时c(OH-)减小、c(H+)=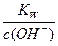 增大这一点。
增大这一点。
练习册系列答案
相关题目
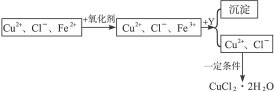
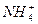 、Cl-、H+、OH-四种离子,下列说法中错误的是( )
、Cl-、H+、OH-四种离子,下列说法中错误的是( )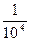 y
y