题目内容
【题目】柴油机氮氧化物(NOx)处理技术是一种系统简单,占用空间较小的柴油车尾气处理技术,氮氧化物主要在催化转化装置中被处理。
(1)柴油中含有多种烷烃,其燃烧性能用十六烷值表示。C16H34完全燃烧的化学方程式是______。
(2)柴油发动机工作时在稀燃(O2充足、柴油较少)和富燃(O2不足、柴油较多)条件下交替进行,催化转化装置中的物质变化如下图所示。
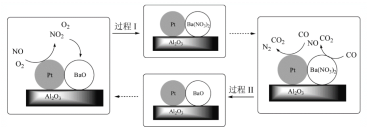
①BaO吸收NO2的化学方程式是______。
②富燃条件下Pt表面反应的化学方程式是______。
(3)研究CO2对BaO吸收氮氧化物的影响,一定温度下,测得气体中CO2的体积分数与氮氧化物吸收率的关系如下图所示。
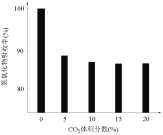
①一定范围内,氮氧化物吸收率随CO2体积分数的增大而下降,原因是_____。
②当CO2体积分数达到10%~20%时,氮氧化物吸收率依然较高,原因可能有:______。
③若柴油中硫含量较高,在稀燃过程中,BaO吸收氮氧化物的能力下降至很低水平,结合化学方程式解释原因:______。
【答案】2C16H34+49O2![]() 32CO2+34H2O 2BaO+4NO2+O2=2Ba(NO3)2 2CO+2NO
32CO2+34H2O 2BaO+4NO2+O2=2Ba(NO3)2 2CO+2NO![]() N2+2CO2 BaO与CO2反应生成BaCO3,覆盖在BaO表面 BaCO3在一定程度上也能吸收NOx 稀燃过程中,柴油中的硫氧化为SO2,2BaO+2SO2+O2=2BaSO4,BaSO4稳定,不易分解,也难与NOx反应
N2+2CO2 BaO与CO2反应生成BaCO3,覆盖在BaO表面 BaCO3在一定程度上也能吸收NOx 稀燃过程中,柴油中的硫氧化为SO2,2BaO+2SO2+O2=2BaSO4,BaSO4稳定,不易分解,也难与NOx反应
【解析】
根据烷烃燃烧通式书写十六烷燃烧的化学方程式;根据图示所给信息写出正确的化学方程式;根据图示所给信息结合反应原理分析相应原因。
(1)十六烷在氧气中充分燃烧生成二氧化碳和水,化学方程式为2C16H34+49O2![]() 32CO2+34H2O;
32CO2+34H2O;
(2)①根据图示,NO2和O2与BaO反应生成Ba(NO3)2,化学方程式为2BaO+4NO2+O2=2Ba(NO3)2;
②根据图示,富燃条件下,NO和CO可以在Pt的催化下反应生成CO2和N2,化学方程式为2CO+2NO![]() N2+2CO2;
N2+2CO2;
(3)①利用BaO吸收汽车尾气中的氮氧化物,随着CO2量的不断增加,BaO对氮氧化物的吸收率逐渐下降,这是由于CO2可以和BaO发生反应生成BaCO3,覆盖在BaO表面,阻止BaO进一步吸收氮氧化物;
②当CO2体积分数达到10%~20%时,BaO对氮氧化物的吸收率虽较无二氧化碳的条件下低,但是吸收率也相对较高,这可能是CO2与BaO反应生成的BaCO3对氮氧化物也有一定的吸收;
③柴油在氧气充足的条件下燃烧为稀燃过程中,稀燃过程会使柴油中的硫氧化为SO2,2BaO+2SO2+O2=2BaSO4,BaSO4稳定,不易分解,也难与NOx反应。

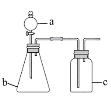
【题目】用如图所示的装置进行实验(夹持及尾气处理仪器略去),能达到实验目的的是
选项 | a中试剂 | b中试剂 | c中试剂 | 实验目的 | 装置 |
A | 氨水 | CaO | 无 | 制取并收集氨气 |
|
B | 浓盐酸 | MnO2 | 饱和NaCl溶液 | 制备纯净的Cl2 | |
C | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 比较酸性强弱: H2CO3>H2SiO3 | |
D | 浓硫酸 | Na2SO3 | KMnO4酸性溶液 | 验证SO2具有还原性 |
A.AB.BC.CD.D
【题目】某化学课外小组为了探究CaCl2溶液和Na2SO4溶液反应有没有限度,设计了如下活动过程,请完成表中空格:(已知CaSO4在水中微溶,CaCO3在水中难溶)
实验步骤 | 向3-4 mL 1 mol/L的CaCl2溶液中滴入1mol/L的Na2SO4溶液至反应完全 |
实验现象 | _____________________ |
离子方程式 | _________________ |
小组讨论 交流 | 向上述反应后的清液中滴入适量1mol/L的Na2CO3 溶液会出现什么现象 |
对于实验现象提出的假设,说明理由 | 假设:①_____________________、②_______________________ 理由:①__________________、②_____________________。 |
实验证明你的假设 | 现象:____________________________________。 |
离子方程式 | _________________ |
解释 | _________________ |
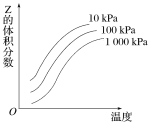
【题目】将一定量的氨基甲酸铵固体置于某容积恒定的真空容器中,发生反应:H2NCOONH4(s)![]() 2NH3(g)+CO2(g),在不同温度下,该反应达平衡状态时的部分数据如表所示。下列说法正确的是( )
2NH3(g)+CO2(g),在不同温度下,该反应达平衡状态时的部分数据如表所示。下列说法正确的是( )
温度 | 平衡浓度(mol·L-1) | |
c(NH3) | c(CO2) | |
T1 | 0.1 | |
T2 | 0.1 | |
A.若T2>T1,则该反应的ΔH<0
B.向容器中充入N2,H2NCOONH4质量增加
C.NH3体积分数不变时,说明该反应达到平衡
D.T1、T2时,转化的H2NCOONH4的物质的量Δn(T2)=2Δn(T1)
【题目】下列选项中的原因或结论与现象不对应的是
选项 | 现象 | 原因或结论 |
A | 在H2O2中加入MnO2,能加速H2O2的分解速率 | MnO2降低了反应所需的活化能 |
B | 在密闭容器中有反应:A+xB(g) | A非气体、x=1 |
C | 将盛有NO2气体的密闭容器浸泡在热水中,容器内气体颜色变深 | 2NO2(g) |
D | 向5mL 0.005mol·L-1 FeCl3溶液中加入5mL 0.015mol·L-1 KSCN溶液,溶液呈红色,再滴加几滴1 mol·L-1 KSCN溶液,溶液颜色加深 | 增大反应物浓度,平衡向正反应方向移动 |
A. A B. B C. C D. D