题目内容
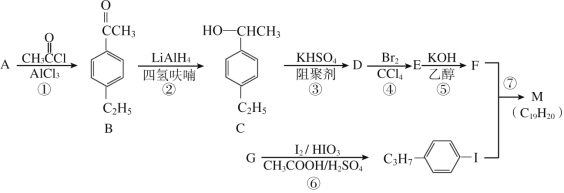
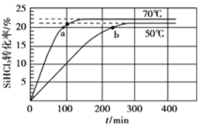
【题目】三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料,在催化剂作用下可发生反应:2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g),在50 ℃和70 ℃时SiHCl3的转化率随时间变化的结果如图所示。下列叙述正确的是
SiH2Cl2(g)+SiCl4(g),在50 ℃和70 ℃时SiHCl3的转化率随时间变化的结果如图所示。下列叙述正确的是
A.正反应方向为放热反应
B.反应速率大小:va <vb
C.70 ℃时,平衡常数K =![]()
D.增大压强,可以提高SiHCl3的平衡转化率,缩短达平衡的时间
【答案】C
【解析】
A. 根据图像,70 ℃时SiHCl3的转化率高于50 ℃,升高温度平衡正向移动,则正反应方向为吸热反应,A错误;
B. 温度越高反应速率越大,则反应速率大小:va >vb,B错误;
C. 70 ℃时,SiHCl3的转化率为22%,根据方程式可知
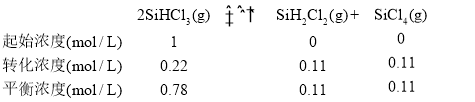
则平衡常数K =![]() ,C正确;
,C正确;
D. 方程式两边气体计量数之和相等,则增大压强,平衡不移动,SiHCl3的平衡转化率不变,反应速率加快,能缩短达平衡的时间,D错误;
答案为C。

练习册系列答案
相关题目