题目内容
下列说法正确的是( )
| A.除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 |
| B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测定 |
| C.制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中 |
| D.加入盐酸可以除去硫酸钠中的少量碳酸钠杂质 |
A
试题分析:铝为两性物质,可以溶于强碱,铁不溶于强碱,所以除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤,故A正确,为本题的答案;瓷坩埚的主要成分中含有二氧化硅,所以能被氢氧化钠破坏,故B的说法是错误的;制备Fe(OH)3胶体,通常是将氯化铁滴入沸水中,故C错误;硫酸钠中的少量碳酸钠杂质与盐酸反应生成了氯化钠,增加了新的杂志,故D的说法是错误的。
点评:本题考查了金属及其化合物、胶体的制备、除杂,这些知识都是高考考查的热点,本题有一定的综合性,难度适中。

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
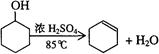
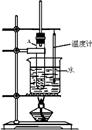
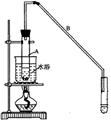
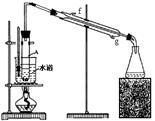
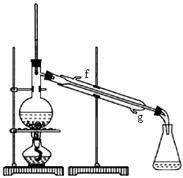
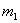 g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案: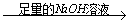 充分反应后测定剩余固体质量
充分反应后测定剩余固体质量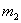 g
g 生成的气体在标准状况下的体积为VL。
生成的气体在标准状况下的体积为VL。