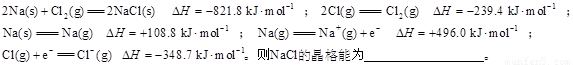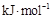题目内容
已知在Na2HPO4溶于水后,它的水解程度远大于电离程度。对于平衡:![]() +H2O
+H2O![]() H3O++
H3O++![]() ,欲使溶液中c(
,欲使溶液中c(![]() )、c(H3O+)、c(
)、c(H3O+)、c(![]() )均下降,可采用的方法是()
)均下降,可采用的方法是()
A.加少量水 B.加热
C.加消石灰 D.加AgNO3
C
解析:
本题考查了![]() 在水中的两个平衡:
在水中的两个平衡:![]() 的电离:
的电离:
![]() +H2O
+H2O![]() H3O++
H3O++![]() ,
,![]() 的水解:
的水解:![]() +H2O
+H2O![]() +OH-。题目中给出了电离方程式,误导答题者忽略前面给出的“水解程度大于电离程度”的已知条件,而误选A。加水稀释后,
+OH-。题目中给出了电离方程式,误导答题者忽略前面给出的“水解程度大于电离程度”的已知条件,而误选A。加水稀释后,![]() 、
、![]() 都减小,忽略了水解为主,溶液呈碱性,稀释时c(OH-)减小、c(H+)=
都减小,忽略了水解为主,溶液呈碱性,稀释时c(OH-)减小、c(H+)=![]() 增大这一点。
增大这一点。

(6分)按要求回答下列问题:
(1)已知在200℃,101kPa时,H2与碘蒸气作用生成1mol HI放出7.45kJ热量,则该反应的热化学方程式为 。
(2)太阳能的开发和利用是21世纪一个重要课题。利用储能介质储存太阳能的原理是:白天在太阳照射下使某种盐熔化,吸收热量,晚间熔盐固化释放出相应能量。已知下列数据:
| 序号 | 盐 | 熔点/℃ | 熔化热/ | 参考价格/ |
| ① | CaCl2·6H2O | 29.0 | 37.3 | 780~850 |
| ② | Na2SO4·10H2O | 32.4 | 77.0 | 800~900 |
| ③ | Na2HPO4·12H2O | 36.1 | 100.1 | 1800~2400 |
| ④ | Na2SiO3·5H2O | 52.5 | 49.7 | 1400~1800 |
其中最适宜作为储能介质的是 。(选填物质序号)
(3)离子晶体晶格能的定义是气态离子形成1mol离子晶体释放的能量,通常取正值。现已知:
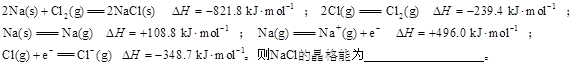
(6分)按要求回答下列问题:
(1)已知在200℃,101kPa时,H2与碘蒸气作用生成1mol HI放出7.45kJ热量,则该反应的热化学方程式为 。
(2)太阳能的开发和利用是21世纪一个重要课题。利用储能介质储存太阳能的原理是:白天在太阳照射下使某种盐熔化,吸收热量,晚间熔盐固化释放出相应能量。已知下列数据:
|
序号 |
盐 |
熔点/℃ |
熔化热/ |
参考价格/ |
|
① |
CaCl2·6H2O |
29.0 |
37.3 |
780~850 |
|
② |
Na2SO4·10H2O |
32.4 |
77.0 |
800~900 |
|
③ |
Na2HPO4·12H2O |
36.1 |
100.1 |
1800~2400 |
|
④ |
Na2SiO3·5H2O |
52.5 |
49.7 |
1400~1800 |
其中最适宜作为储能介质的是 。(选填物质序号)
(3)离子晶体晶格能的定义是气态离子形成1mol离子晶体释放的能量,通常取正值。现已知: