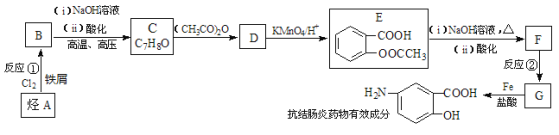
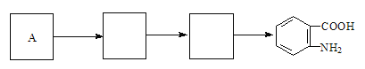
题目内容
【题目】某些资料认为:NO、NO2不能与Na2O2反应。某小组学生提出质疑,他们从理论上分析过氧化钠和二氧化氮都有氧化性,根据化合价升降原则提出假设:
假设Ⅰ.过氧化钠氧化二氧化氮
假设Ⅱ.二氧化氮氧化过氧化钠
(1)小组甲同学设计实验如下:
①试管A中反应的化学方程式是 。
②待试管B中收集满气体,向试管B中加入适量 Na2O2粉末,塞紧塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的小木条迅速伸进试管内,发现木条复燃。甲同学认为假设Ⅱ正确;乙同学认为该装置不能达到实验目的。为准确达到实验目的,需在A、B之间增加一个装置,该装置的作用是 。
③乙同学用改进后装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;余烬木条未复燃。得出结论:假设Ⅰ正确。NO2和Na2O2反应的方程式是 。
(2)丙同学认为NO易与O2发生反应,应更易被Na2O2氧化。
查阅资料:①2NO+Na2O2=2NaNO2
②6NaNO2+3H2SO4=3Na2SO4+2HNO3+4NO↑+2H2O;
③酸性条件下,NO或NO2–都能与MnO4–反应生成NO3–和Mn2+
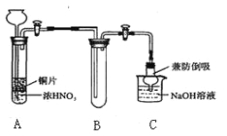
丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。

①B中观察到的主要现象是 ,F装置的作用是 。
②在反应前,打开弹簧夹,通入一段时间N2,目的是 。
③充分反应后,检验D装置中反应产物的实验方法是 。
【答案】(1)①Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
②除去生成NO2气体中混有的水蒸气;③Na2O2+2NO2=2NaNO3(2分)
(2)①铜片逐渐溶解,溶液变为蓝色,有无色气泡产生;(2分)
吸收未反应的NO(2分)
②将装置中的空气排出(2分)
③取D装置中产物少许,加入稀硫酸,若产生无色气体,遇到空气变为红棕色,产物是亚硝酸钠;若无明显现象则为硝酸钠。(3分)
【解析】
试题分析:(1)①Cu与浓硝酸反应生成二氧化氮、硝酸铜和水,其反应的化学方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;
②Cu与浓硝酸反应生成二氧化氮中含有水蒸气,水蒸气能与过氧化钠反应生成氧气,所以要在A、B之间增加一个装置干燥装置,除去生成NO2气体中混有的水蒸气;
③若过氧化钠氧化二氧化氮,则生成硝酸钠,其反应的化学方程式为:Na2O2+2NO2=2NaNO3;
(2)①在B装置中二氧化氮与水反应生成稀硝酸,稀硝酸与Cu反应生成NO,所以B中观察到的主要现象是:铜片逐渐溶解,溶液变为蓝色,有无色气泡产生;NO是有毒气体要进行尾气处理,由题中的信息可以NO能被酸性高锰酸钾吸收;
②空气中的氧气能氧化NO,实验时要排尽装置中的空气,所以在反应前,打开弹簧夹,通入一段时间N2,目的是:将装置中的空气排出;
③亚硝酸钠中加盐酸会生成NO,NO遇到空气中的氧气会变为红棕色,则检验D装置中物质的方法为:取D装置中产物少许,加入稀盐酸,若产生无色气体,遇到空气变为红棕色,产物是亚硝酸钠,反之为硝酸钠。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案