题目内容
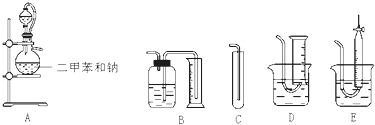
【题目】I. A、B、C、D四种均为含有钠元素的化合物,A、B、C与盐酸反应均可生成D;加热固体C可生成A和一种无色无味的气体X;在A溶液中通入足量X,又可生成C; B溶液和C溶液混合可生成A。请回答:
(1)A是___________,B是___________,C___________,D是___________,(均用化学式表示)
(2)写出上述反应中由A生成C的化学方程式:____________________________________。
(3)写出物质C的一种常见用途:____________________________________。
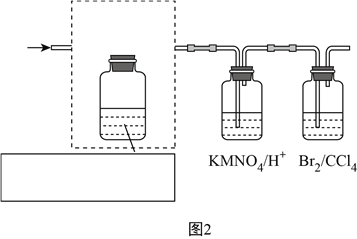
Ⅱ.化合物甲仅含两种元素。B为黄绿色气体,气体D能使湿润的红色石蕊试纸变蓝色。在一定条件下有如下转化关系:

请回答:
(1)化合物甲所含元素为__________(请填写元素符号),甲的化学式为_____________________。
(2)气体B与水反应的离子方程式为____________________________________。
(3)甲与水反应的化学方程式为____________________________________。
【答案】 Na2CO3 NaOH NaHCO3 NaCl Na2CO3+CO2+H2O=2NaHCO3 作发酵粉或治疗胃酸过多的药剂均可 N、Cl NCl3 Cl2+H2O![]() H++Cl-+HClO NCl3+3H2O=NH3+3HClO
H++Cl-+HClO NCl3+3H2O=NH3+3HClO
【解析】I. 三种含钠元素的化合物A、B、C都能与盐酸反应生成D,则D为NaCl,加热固体C可生成A和一种无色无味的气体X,说明C不稳定,在A溶液中通入足量X,又可生成C,所以C为NaHCO3,A为Na2CO3,X为CO2,NaHCO3与NaOH反应可生成Na2CO3,所以B为NaOH。则:
(1)根据上述分析,则A是Na2CO3,B是NaOH,C是NaHCO3,D是NaCl;
(2) 由A生成C的化学方程式为Na2CO3+CO2+H2O=2NaHCO3;
(3) NaHCO3常见用途有作发酵粉或治疗胃酸过多等;
Ⅱ. B为黄绿色气体,即氯气,气体D能使湿润的红色石蕊试纸变蓝色,则D为NH3,所以甲中含有的两种元素是N元素和Cl元素,由转化关系可知,甲与水反应生成的D是NH3,则E中含有氧元素,又Cl2与水反应生成盐酸和次氯酸,次氯酸中含有氧元素,所以E为次氯酸,则F为盐酸, 12.05g的甲分解生成1.4g的N2和氯气,则n(N2) =0.05mol,氯气的质量为10.65g,即n(Cl2) =0.15mol,所以甲的化学式为NCl3。则:
(1)化合物甲所含元素为N和Cl,甲的化学式为NCl3;
(2) Cl2与水反应的离子方程式为Cl2+H2O![]() H++Cl-+HClO;
H++Cl-+HClO;
(3)甲与水反应的化学方程式NCl3+3H2O=NH3+3HClO

 阅读快车系列答案
阅读快车系列答案【题目】在一个盛有催化剂容积可变的密闭容器中,保持一定的温度和压强,进行以下反应:N2+3H22NH3 . 已知加入1molN2和4molH2时,达到平衡后生成amolNH3 . 有恒温恒压下欲保持平衡时各组分的体积分数不变.填表(恒温恒压)
已知 | 起始状态物质的量/mol | 平衡时NH3的 | ||
N2 | H2 | NH3 | ||
1 | 4 | 0 | a | |
① | 1.5 | 9 | 0 | |
② | 1 | 0.5a | ||
③ | m | g(g≥4m) | 0 | |