题目内容
【题目】过氧化氢H2O2(氧的化合价为﹣1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl===2NaCl+H2O2
B.Ag2O+H2O2===2Ag+O2↑+H2O
C.2H2O2===2H2O+O2 ↑
D.3H2O2+Cr2(SO4)3+10KOH===2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是_________(填代号);H2O2既体现氧化性又体现还原性的反应是_________(填代号)。
(2)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应。
氧化反应:H2O2﹣2e﹣===2H++O2↑
还原反应:MnO4-+5e﹣+8H+===Mn2++4H2O
写出该氧化还原反应的离子方程式:___________________。
(3)上面实验中用到一定物质的量浓度的稀硫酸,若配制1mol/L的稀硫酸溶液480mL,需用18mol/L浓H2SO4____mL,配制中需要用到的主要玻璃仪器是(填序号)______。A.100mL量筒 B.托盘天平 C.玻璃棒 D.100mL容量瓶 E.50mL 量筒 F.胶头滴管 G.烧杯 H.500mL容量瓶
(4)下面操作造成所配稀硫酸溶液浓度偏高的是______________
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
(5)如图是一种用电解原理来制备H2O2,并用产生的H2O2处理废氨水的装置。
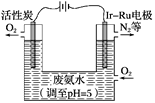
①为了不影响H2O2的产量,需要向废氨水中加入适量HNO3调节溶液的pH约为5,则所得溶液中c(NH4+)________(填“>”“<”或“=”)c(NO3-)。
②Ir-Ru惰性电极吸附O2生成H2O2,其电极反应式为:______________________。
③理论上电路中每转移3 mol e-,最多可以处理废氨水中溶质(以NH3计)的质量是________g。
【答案】D C 2MnO4-+5H2O2+6H+===2Mn2++8H2O+5O2↑ 27.8 CEFGH ACD < O2+2H++2e-===H2O2 17
【解析】
(1)A、根据反应没有化合价的变化,不属于氧化还原反应;B、根据化学反应方程式,Ag2O为氧化剂,H2O2为还原剂,H2O2体现还原性;C、H2O2既是氧化剂又是还原剂,既体现氧化性又体现还原性;D、H2O2只体现氧化性;H2O2仅体现氧化性的是D;既体现氧化性又体现还原性的是C;(2)氧化还原反应中得失电子数目守恒,因此该反应的离子方程式为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑;(3)稀释前后溶质物质的量不变,实验室没有480mL的容量瓶,应用500mL容量瓶,因此有500×10-3×1=V(H2SO4)×10-3×18,解得V(H2SO4)=27.8mL;配制时需要的仪器有量筒、胶头滴管、烧杯、玻璃棒、500mL容量瓶,即CEFGH;(4)根据c=n/V=m/MV,A、溶解后溶液没有冷却到室温就转移,定容后冷却到室温后,溶液体积减小,所配溶液浓度偏高,A符合题意;B、转移时没有洗涤烧杯和玻璃棒,造成容量瓶中溶质的物质的量或质量减小,所配溶液浓度偏低,B不符合题意;C、定容时俯视液面,容量瓶中溶液的体积偏小,浓度偏高,C符合题意;D、量筒洗涤后转移到容量瓶中,容量瓶中的溶质的质量或物质的量偏高,所配浓度偏高,D符合题意;E、定容后、摇匀再加蒸馏水,对溶液稀释,浓度偏低,E不符合题意;综上所述,符合题意的是ACD;(5)①根据溶液呈现电中性,即有c(NH4+)+c(H+)=c(OH-)+c(NO3-),溶液的pH=5,有c(H+)>c(OH-),推出c(NO3-)>c(NH4+);②O2得到电子,转化成H2O2,发生还原反应,电极反应式为O2+2H++2e-=H2O2;③根据题意,NH3中N转化成N2,每转移3mole-,消耗NH3的物质的量为1mol,即处理NH3的质量为17g。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案