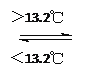题目内容
【题目】海洋资源的利用具有广阔前景。
(1)下图是从海水中提取镁的简单流程。
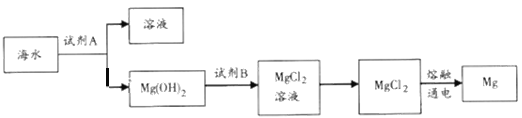
①工业上常用于沉淀Mg2+的试剂A是__________(填化学式),Mg(OH)2转化为MgCl2的离子方程式为________________________。
②由无水MgCl2制取Mg的化学方程式是______________________。
(2)海带灰中富含以I-形式存在的碘元素,实验室提取I2的途径如下所示:
![]()
①灼烧海带至灰烬时所用的主要仪器是__________(填名称);
②向酸化的滤液中加过氧化氢溶液,该反应的离子方程式为__________;
③反应结束后,加入CCl4作萃取剂,采用萃取-分液的方法从碘水中提取碘,主要操作步骤如下图:
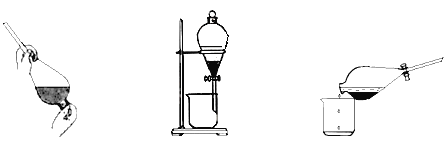
甲.加入萃取剂后振荡 乙.静置分层 丙.分离
甲、乙、丙3步实验操作中,错误的是__________(填“甲”、“乙”或“丙”)。
(3)海水中部分离子的含量如下:
成分 | 含量(mg/L) | 成分 | 含量(mg/L) |
Na+ | 10560 | Cl- | 18980 |
Mg2+ | 1272 | Br- | 64 |
Ca2+ | 400 | SO42- | 2560 |
若从100L该海水中提取镁,理论上需加入试剂A__________g。
【答案】Ca(OH)2 Mg(OH)2+ 2H+= Mg2++H2O MgCl2(熔融) ![]() Mg+Cl2↑ 坩埚 2H++H2O2+2I-=I2+2H2O 丙 392.2g
Mg+Cl2↑ 坩埚 2H++H2O2+2I-=I2+2H2O 丙 392.2g
【解析】
(1)①工业上用可溶性碱与镁离子反应生成 Mg(OH)2,所以工业上常用于沉淀Mg2+的试剂A是Ca(OH)2,氢氧化镁是碱,能与酸反应生成镁盐和水,则Mg(OH)2转化为MgCl2的离子方程式是Mg(OH)2+ 2H+= Mg2++H2O;
②氯化镁是离子化合物,由无水MgCl2制取Mg的化学方程式是MgCl2(熔融) ![]() Mg+Cl2↑;
Mg+Cl2↑;
(2)①坩埚可以加强热,所以灼烧固体用坩埚;
②过氧化氢具有氧化性,碘离子具有还原性,在酸性溶液中发生氧化还原反应生成碘单质和水,该反应的离子方程式为2H++H2O2+2I-=I2+2H2O;
③ 在萃取、分液操作中,分液时,先把下层液体从分液漏斗的下口流出,然后上层液体从分液漏斗上口倒出,所以甲、乙、丙3步实验操作中,不正确的是丙;
(3)根据表中数据可知Mg2+的物质的量浓度是![]() ;100L的海水中Mg2+的含量=0.053mol/L
;100L的海水中Mg2+的含量=0.053mol/L![]() 100L=5.3mol,加入A即氢氧化钙发生沉淀反应,1mol Mg2+需要1mol氢氧化钙完全沉淀,因此若从100L的海水中提取镁,理论上加入沉淀剂氢氧化钙的质量=5.3mol
100L=5.3mol,加入A即氢氧化钙发生沉淀反应,1mol Mg2+需要1mol氢氧化钙完全沉淀,因此若从100L的海水中提取镁,理论上加入沉淀剂氢氧化钙的质量=5.3mol![]() 74g/mol=392.2g。
74g/mol=392.2g。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案【题目】依据题意,完成下列各题:
(1)1.0 g乙醇完全燃烧生成液态水放出1.37 kJ热量,表示乙醇的燃烧热的热化学方程式为__________________________________________________;
(2) “长征”2号火箭的发动机中用“偏二甲肼”(分子式为C2H8N2)和四氧化二氮作为液态燃料。已知a g偏二甲肼与b g四氧化二氮在发动机内燃烧生成稳定的、对环境友好的物质。若生成1 mol N2(g) 的反应热为c kJ,写出热化学方程式______________________________________________;
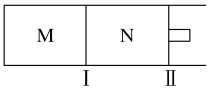
(3) T ℃时,如图所示, 对应的化学方程式为______________________;
(4) 向足量的H2SO4溶液中加入100 mL 0.4 mol·L-1的Ba(OH)2溶液,放出的热量是5.12 kJ。向足量的Ba(OH)2溶液中加入100 mL 0.4 mol·L-1的HCl溶液,放出的热量为2.2 kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为Ba2+(aq)+SO42-(aq)===BaSO4(s) ΔH=______________;
(5) 研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键时所需吸收的能量。下表是部分化学键的键能数据:
化学键 | P—P | P—O | O==O | P==O |
键能kJ/mol | 197 | 360 | 499 | x |
已知白磷(P4)的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物(P4O10)的结构如图所示,则上表中x=_________________。