题目内容
下列实验方法合理的是
| A.可用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液 |
| B.可用分液的方法从溶有溴的四氯化碳溶液中分离出单质溴 |
| C.为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量相等 |
| D.可用水鉴别已烷、四氯化碳、乙醇三种无色液体 |
D
略

练习册系列答案
相关题目
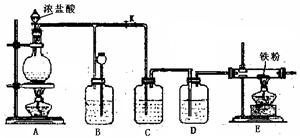
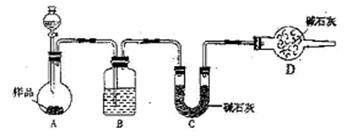
 (4)E处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是 ,B的作用是 。
(4)E处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是 ,B的作用是 。
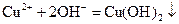 ,将
,将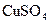 溶液滴入氨水中,振荡,会产生蓝色沉淀
溶液滴入氨水中,振荡,会产生蓝色沉淀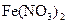 溶液中存在平衡:
溶液中存在平衡: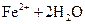
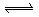
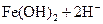 ,加入少量稀盐酸后溶液浅绿色会加深
,加入少量稀盐酸后溶液浅绿色会加深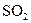 有漂白性,将
有漂白性,将


