题目内容
氧化还原反应与四种基本反应类型的关系如下图所示,则下列化学反应属于丙区域的是( )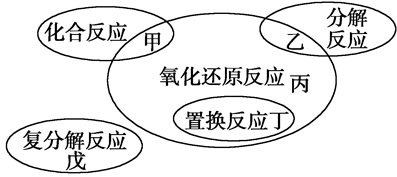
| A.Cl2+2KBr=Br2+2KCl | B.2NaHCO3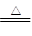 Na2CO3+H2O+CO2↑ Na2CO3+H2O+CO2↑ |
C.3Mg+N2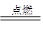 Mg3N2 Mg3N2 | D.2Na2O2+2CO2=2Na2CO3+O2 |
D
解析试题分析:A,是置换反应,属于丁区。B是分解反应,属于戊区。C.是化合反应,属于甲区。D不属于任何基本反应类型,但实质是氧化还原反应。属于丙区。
考点:考查基本反应类型与氧化还原反应的关系的知识。

练习册系列答案
相关题目
在3S + 6KOH = 2K2S + K2SO3 + 3H2O 反应中,做氧化剂的S原子与做还原剂的S原子的物质的量之比是( )
| A.1:2 | B.2:1 | C.1:3 | D.3:1 |
将0.39g锌粉加入到20.0 mL的0.200 mol·L-1 MO2+溶液中,恰好完全反应,则还原产物可能是
| A.M+ | B.M2+ | C.M3+ | D.MO42- |
实验室制取少量N2,常利用的反应是:NaNO2+NH4Cl NaCl+N2↑+2H2O,关于该反应的说法正确的是
NaCl+N2↑+2H2O,关于该反应的说法正确的是
| A.NaNO2是氧化剂,发生还原反应 |
| B.生成1mol N2时转移的电子数为6mol |
| C.NH4Cl中的N元素被还原 |
| D.N2既是氧化剂又是还原剂 |
在KClO3+6HCl KCl+3Cl2↑+3H2O中,被还原的氯元素和被氧化的氯元素的
KCl+3Cl2↑+3H2O中,被还原的氯元素和被氧化的氯元素的
物质的量之比是
| A.1 : 6 | B.1 : 5 | C.5 : 1 | D.6 : 1 |
在8NH3+3Cl2=N2+6NH4Cl反应中,在该反应中氧化剂和还原剂的分子个数之比是( )。
| A.3:1 | B.3:8 | C.3:2 | D.8:3 |
已知某反应中反应物与生成物有:KIO3、Na2SO3、H2SO4、I2、K2SO4、H2O 和未知物X。下列说法中不正确的是
| A.该未知物X为Na2SO4 |
| B.该反应的氧化剂是KIO3 |
| C.该反应中,发生氧化反应的过程是KIO3→I2 |
| D.由反应可知还原性强弱顺序为:Na2SO3>I2 |
根据表中信息,判断下列叙述中正确的是
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | | Cl- |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
B.氧化性强弱的比较:KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O
已知反应:①Cl2+2KBr=2KCl+Br2,②KClO3 +6HCl=3Cl2+KCl +3H2O,③2KBrO3 +Cl2=Br2+2KClO3,下列说法正确的是
| A.上述三个反应都有单质生成,所以都是置换反应 |
| B.反应②中氧化剂与还原剂的物质的量之比为6∶1 |
| C.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2 |
| D.反应③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol |