题目内容
1.铁是自然界分布最广的金属元素之一,在地壳中的质量约占5%左右.铁矿石的种类很多,重要的有磁铁矿石(主要成分是Fe3O4)、赤铁矿石(主要成分是Fe2O3)等.(1)写出赤铁矿炼铁的主要化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)红热的铁能跟水蒸气反应,有一种产物是可燃性气体,则其反应式为3Fe+4H2O(气)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
在常温下,铁跟水不起反应.但是,在水和空气里的氧气及二氧化碳等的共同作用下,铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一.刷油漆是重要的防腐蚀措施之一,油漆防腐蚀的主要原理是将金属与空气和水隔离.
(3)铁元素是人体的重要营养元素,举一例说明铁元素在人体中的重要作用.血红素中含铁,人体缺铁会造成贫血.
分析 (1)赤铁矿炼铁,发生氧化铁与CO的氧化还原反应;
(2)红热的铁能跟水蒸气反应,生成气体为氢气,还生成四氧化三铁;油漆防腐蚀可使铁隔绝空气、水;
(3)体缺铁会造成贫血.
解答 解:(1)赤铁矿炼铁,发生氧化铁与CO的氧化还原反应,反应为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)红热的铁能跟水蒸气反应,生成气体为氢气,还生成四氧化三铁,反应为3Fe+4H2O(气)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,油漆防腐蚀的主要原理是将金属与空气和水隔离,
故答案为:3Fe+4H2O(气)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;将金属与空气和水隔离;
(3)铁元素在人体中的重要作用如血红素中含铁,人体缺铁会造成贫血,故答案为:血红素中含铁,人体缺铁会造成贫血.
点评 本题考查铁的化学性质,为高频考点,把握铁及其化合物的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
19.某温度下,0.02mol•L-1NaHSO3溶液的pH=3.下列说法正确的是( )
| A. | 加水稀释10倍后,溶液的pH=4 | |
| B. | c(SO32-)+c(OH-)=c(H2SO3)+c(HSO3-) | |
| C. | 2c(SO32-)+c(HSO3-)+c(H2SO3)=0.02mol•L-1 | |
| D. | $\frac{c({H}^{+})•c(S{{O}_{3}}^{2-})}{c(HS{{O}_{3}}^{-})}$约为5×10-5 mol•L-1 |
12.下列反应一定能自发进行的是( )
| A. | 放热反应 | B. | 熵增加的反应 | ||
| C. | 熵增加的吸热反应 | D. | 熵增加的放热反应 |
9.在A、B、C、D四个烧杯内分别放入0.1mol的Na、Na2O、Na2O2、NaOH,然后各加入100mL H2O,搅拌使固体完全溶解,则A、B、C、D的质量分数大小顺序为( )
| A. | A<B<C<D | B. | D<A<B=C | C. | A=D<B=C | D. | D<A<B<C |
13.下列说法正确的是( )
| A. | SO2和SO3都是酸性氧化物,二者的水溶液都是强酸 | |
| B. | 将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化 | |
| C. | 硫粉在过量的纯氧中燃烧可以生成大量的SO3 | |
| D. | 富含硫黄的矿物在工业上可用于制造硫酸 |
10.下列化合物分别跟溴在铁粉作催化剂的条件下反应,苯环上的氢原子被取代,所得一溴代物有三种同分异构体的是( )
①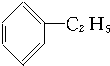 ②
②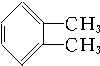 ③
③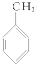 ④
④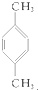
①
 ②
② ③
③ ④
④
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |