��Ŀ����
����Ŀ��EDTA(�Ҷ���������)��һ������Ca2+��Mg2+�Ƚ�ϵ����ϼ���ij�����о���ѧϰС����ʵ�����Ʊ�EDTA��������ⶨij����ˮ��Ӳ�ȡ��Ʊ�EDTA��ʵ�鲽�����£�

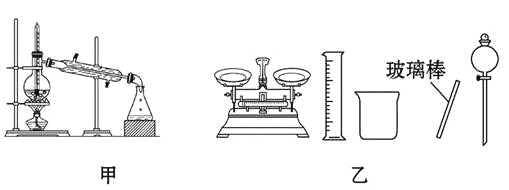
����1����ȡ94.5g(1.0mol)ClCH2COOH��1000mL������ƿ��(��ͼ)����������50%Na2CO3��Һ�������ٲ�����ɫ���ݣ�
����2������15.6g(0.26mol)H2NCH2CH2NH2��ҡ�ȣ�����Ƭ�̣�����2.0mol��L-1NaOH��Һ90mL����ˮ�������Ϊ600mL���ң��¶ȼ�50�����2h��
����3����ȴ�����ձ��У��������̿��ɫ�����衢���á����ˡ������������Һ��pH=1���а�ɫ�������ɣ����ˣ�����Ƶ�EDTA�������ˮӲ�ȣ�ȡ����ˮ��Ʒ250mL����Ԥ��������EDTA���м�⡣ʵ�����漰�ķ�Ӧ��M2+(��������)+Y4-(EDTA)=MY2-��M2+(��������)+EBT(����T����ɫ)=MEBT(�ƺ�ɫ)��MEBT+Y4-(EDTA)=MY2-+EBT(����T)��
�ش��������⣺
��1������1�з�����Ӧ�����ӷ���ʽΪ_____��
��2������Q��������_____����ȴˮ��_____�ӿ�(����x������y��)������
��3����NaOH������������NaOH��Һ������ʱʹ�õ�������������ƽ��ҩ�ס��ձ�����������_____��_____����Ҫ����NaOH���������Ϊ_____��
��4�����������ˮ��ת�Ƶ���ƿ�У����백ˮ-�Ȼ�炙�����Һ����pHΪ10���μӼ��θ���T��Һ����0.0100mol��L-1EDTA����Һ���еζ���
��ȷ�ϴﵽ�ζ��յ��������_____��
�ڵζ��յ�ʱ������EDTA��Һ15.0mL����õ���ˮ��Ӳ��=_____��(ˮӲ�ȵı�ʾ�����ǽ�ˮ�е�Ca2+��Mg2+������Ca2+�������������CaO��������ͨ����1Lˮ�к���10mgCaO��Ϊ1��)��
����ʵ��ʱװ��EDTA��Һ�ĵζ���ֻ������ˮϴ�Ӷ�δ�ñ�Һ��ϴ����ⶨ�����_____ (����ƫ����ƫС��������Ӱ����)��
���𰸡�2ClCH2COOH��CO32-=2ClCH2COO-��CO2����H2O ���������� x ��ͷ�ι� 100mL����ƿ 8.0g ��Һ�ɾƺ�ɫ��Ϊ��ɫ���Ұ�����ڲ��ָ�ԭɫ 3.36 ƫ��
��������
(1)ClCH2COOH��COOH����̼���Ʒ�Ӧ��
(2)QΪ���������ܣ���ˮ�½��ϳ��ɳ��������ܣ�
(3)�ܽ��ת�Ƶ�250mL����ƿ�ж��ݣ����m��cVM���㣻
(4)�ٵζ�ǰ��ҺΪ�ƺ�ɫ���ζ�������Ϊ��ɫ��������Һ��ɫ�仯Ϊ�ƺ�ɫ��Ϊ��ɫ��
����0.0100molL1��EDTA����Һ���еζ����ζ��յ�ʱ������EDTA��Һ15.00mL����n(M2��)��n(EDTA)��0.0100molL1��15.00��103L��1.5��104mol����25mLˮ��m(CaO)��nM��56g/mol��1.5��104mol��8.2mg����1Lˮ�к���10mg CaO��Ϊ1�ȣ��Դ˼���õ���ˮ��Ӳ�ȣ�
��ʵ��ʱװ��EDTA��Һ�ĵζ���ֻ������ˮϴ�Ӷ�δ�ñ�Һ��ϴ�����ı�Һ���ƫ��
(1)����1�з�����Ӧ�����ӷ���ʽΪ2ClCH2COOH��CO32-=2ClCH2COO-��CO2����H2O��
(2)����Q�����������������ܣ���ȴˮ��x�ӿ�������
(3)��NaOH������������NaOH��Һ������ʱʹ�õ���������ƽ���ձ�������������ͷ�ιܺ�100mL����ƿ����Ҫ����NaOH���������Ϊ0.1L��2.0mol/L��40g/mol��8.0g��
(4)�ٵζ�ǰ��ҺΪ�ƺ�ɫ���ζ�������Ϊ��ɫ����ζ��յ�����Ϊ�������һ��EDTA��Һ����Һ��ɫ�ɾƺ�ɫ��Ϊ��ɫ���Ұ�����ڲ��ָ�ԭɫ��
����0.0100molL1��EDTA����Һ���еζ����ζ��յ�ʱ������EDTA��Һ15.00mL����n(M2��)��n(EDTA)��0.0100molL1��15.00��103L��1.5��104mol����25mLˮ��m(CaO)��nM��56g/mol��1.5��104mol��8.2mg������1Lˮ��m(CaO)��8.2mg��![]() ��336mg��ͨ����1Lˮ�к���10mg CaO��Ϊ1�ȣ����Ըõ���ˮ��Ӳ��Ϊ
��336mg��ͨ����1Lˮ�к���10mg CaO��Ϊ1�ȣ����Ըõ���ˮ��Ӳ��Ϊ![]() ��3.36�ȣ�
��3.36�ȣ�
��ʵ��ʱװ��EDTA��Һ�ĵζ���ֻ������ˮϴ�Ӷ�δ�ñ�Һ��ϴ�����ı�Һ���ƫ����ⶨ�����ƫ��

 �����Ļ�������ҵϵ�д�
�����Ļ�������ҵϵ�д�����Ŀ��ij�¶��£���4.0 L�����ܱ������г���2.0 mol PCl5����ӦPCl5(g) ![]() PCl3(g)��Cl2(g)��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
PCl3(g)��Cl2(g)��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
ʱ��/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
����˵����ȷ����(����)
A.��Ӧ��ǰ50 s��ƽ����Ӧ����Ϊv(PCl3)��0.006 4 mol/(L��s)
B.��ͬ�¶��£���ʼʱ��������г���4.0 mol PCl3��4.0 mol Cl2���ﵽƽ��ʱ��PCl3��ת����С��80%
C.��ͬ�¶��£���ʼʱ��������г���2.0 mol PCl5��0.4 mol PCl3��0.40 mol Cl2���ﵽƽ��ǰv(��)>v(��)
D.���������������䣬�����¶ȣ�ƽ��ʱ��c(PCl3)��0.11 mol/L����Ӧ����H<0