题目内容
19.请判断在下列物理变化过程中,化学键被破坏的是( )| A. | 碘升华 | B. | 溴蒸气被木炭吸附 | ||
| C. | 葡萄糖在水中的扩散 | D. | 氯化钠晶体溶于水 |
分析 分子晶体发生升华、吸附等物理变化时以及非电解质的溶解过程,化学键没有变化,变化的是分子间作用力,离子晶体在熔化状态下电离,离子键被破坏.
解答 解:A.碘升华过程中,化学键没有变化,变化的是分子间作用力,故A错误;
B.溴蒸气被木炭吸附,化学键没有变化,变化的是分子间作用力,故B错误;
C.葡萄糖在水中的扩散,没有发生电离,化学键没有变化,变化的是分子间作用力,故C错误;
D.氯化钠属于离子晶体,溶于水时离子键被破坏,故D正确.
故选D.
点评 本题考查晶体类型的判断,为高频考点,侧重于基本概念的理解,题目难度不大,注意晶体类型的分类和性质的区别.

练习册系列答案
相关题目
9.目前我国城市公布的空气质量报告中的污染物一般不涉及( )
| A. | S02 | B. | N02 | C. | C02 | D. | 可吸入颗粒物 |
10.化学反应可视为旧化学键断裂和新化学键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知:N≡N键的键能是a kJ•mol-1,H-H键的键能是b kJ•mol-1;由N2和H2合成1mol NH3时可放出ckJ的热量.那么N-H键的键能是( )
| A. | $\frac{(a+3b-2c)}{2}$kJ•mol-1 | B. | $\frac{(a+3b+2c)}{6}$kJ•mol-1 | ||
| C. | $\frac{(a+3b-2c)}{6}$kJ•mol-1 | D. | $\frac{(a+3b+2c)}{3}$kJ•mol-1 |
7.下列物质均有漂白作用,其漂白原理相同的是( )
①过氧化钠 ②次氯酸 ③二氧化硫 ④活性炭 ⑤臭氧.
①过氧化钠 ②次氯酸 ③二氧化硫 ④活性炭 ⑤臭氧.
| A. | ①②③ | B. | ①③⑤ | C. | ①②⑤ | D. | ②③④ |
4.下列说法正确的是( )
| A. | HF、HCl、HBr、HI的热稳定性依次减弱与分子间作用力有关 | |
| B. | 因为亚硫酸比碳酸的酸性强,所以硫的非金属性比碳强 | |
| C. | Li、B、Be、C、N、O、F 原子序数依次增大 | |
| D. | 乙醇与二甲醚互为同分异构体 |
8.原子结构模型的演变,经历了五个阶段.其中提出“原子轨道”模型的科学家是( )
| A. | 道尔顿 | B. | 卢瑟福 | C. | 玻尔 | D. | 汤姆生 |
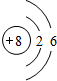 ;B在周期表的位置为第二周期ⅣA族;
;B在周期表的位置为第二周期ⅣA族;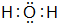 ;
;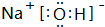 ;
;