题目内容
下面是测定硫酸铜结晶水的实验,请按要求填空。
(1)加热前应将晶体放在________中研碎,加热是放在________中进行,加热失水后,应放在________中冷却。
(2)判断是否完全失去结晶水的方法是________。
(3)做此实验,最少应进行称量操作次________。
(4)下面是某学生的一次实验数据,完成计算,填入表的空格中。
|
坩埚质量 |
坩埚与晶体总质量 |
加热后坩埚与固体总质量 |
测得晶体中结晶水个数 |
误差(偏高或偏低) |
|
11.17 g |
22.7 g |
18.6 g |
|
|
(5)这次实验中产生误差的原因可能是________(填A、B、C、D)造成的。
A.硫酸铜晶体中含不挥发性杂质
B.加热过程中有晶体溅失
C.实验前晶体表面潮湿存水
D.最后两次称量质量相差较大
答案:
解析:
提示:
解析:
(1)研钵;坩埚;干燥器
(2)加热后最后两次称量误差不超过0.1g
(3)4
(4)5:3,偏高
(5)B、C
提示:
设结晶硫酸铜为CuSO4•xH2O,
则:![]()

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:
实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:请回答:
(1)实验中取一定量Cu片和一定量浓H2SO4放在圆底烧瓶中共热,至反应结束后,发现烧瓶中还有少量Cu剩余,则H2SO4 是否剩余
(2)向反应后的溶液中加入足量的CuO,过滤后将滤液加热浓缩,冷却结晶制得硫酸铜晶体(CuSO4?XH2O)某小组同学采用加热法测定该晶体里结晶水X的值;
①冷却结晶后要获得较纯净的硫酸铜晶体采取的操作是
②在他们的每一次实验操作中至少称量
③加热法测定该晶体里结晶水X的值,结晶水完全失去的判断方法是
④下面是三次实验数据的平均值
| 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 11.7g | 22.7g | 18.6g |
(3)装置乙的作用是:
(4)下列说法正确的是:
a.甲装置使用的玻璃仪器有:酒精灯、玻璃管、长颈漏斗、圆底烧瓶
b.KMnO4溶液用于尾气处理
c.当把品红溶液滴入到锥形瓶中,若品红不褪色,说明无NaHSO3产生
d.当把品红溶液滴入到锥形瓶中,若品红褪色,说明NaOH已完全转化为NaHSO3
e.若把品红溶液换成酸性高锰酸钾溶液,并滴入到锥形瓶中,不显紫红色,说明NaOH已完全转化为NaHSO3.
 实验室用浓硫酸与铜的反应制取少量 NaHSO3,实验装置如图所示.请回答:
实验室用浓硫酸与铜的反应制取少量 NaHSO3,实验装置如图所示.请回答: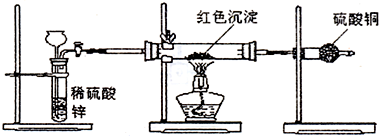
 实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:
实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示: 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.