题目内容
【题目】化合物E是一种医药中间体,常用于制备抗凝血药,合成路线如下:

(1)A的结构简式为__________________________ ;
B中含氧官能团名称为______________、_______________;
(2)C转化为D的反应类型是_______________;
(3)写出D与足量NaOH溶液完全反应的化学方程式___________________________。
(4)1molE最多可与________molH2加成。
(5)写出同时满足下列条件的B的一种同分异构体的结构简式 __________________;
A.能发生银镜反应 B.核磁共振氢谱只有4个峰
C.能与FeCl3溶液发生显色反应,水解时1mol可消耗3molNaOH
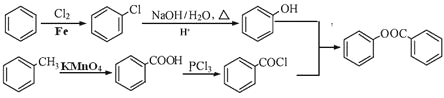
(6)已知工业上以氯苯水解制取苯酚,而酚羟基一般不易直接与羧酸酯化。苯甲酸苯酚酯(![]() )是一种重要的有机合成中间体。结合上述合成路线中有关信息,试写出以苯、甲苯为原料制取苯甲酸苯酚酯的合成路线流程图(无机原料任选)。合成路线流程图示例如下:
)是一种重要的有机合成中间体。结合上述合成路线中有关信息,试写出以苯、甲苯为原料制取苯甲酸苯酚酯的合成路线流程图(无机原料任选)。合成路线流程图示例如下:
![]() _________________________________________________________________________
_________________________________________________________________________
【答案】 CH3CHO 羟基 羧基 取代反应  4
4 ![]()
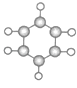
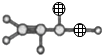
【解析】试题分析:(1)流程图中![]() 可以推断,A为乙醛,结构简式为:CH3CHO,B中含有官能团为羟基、羧基,答案为:CH3CHO,羟基、羧基;(2)C转化为D的反应类型是取代反应,答案为:取代反应;(3)1molD最多可以和3molNaOH反应,反应的化学方程式为:
可以推断,A为乙醛,结构简式为:CH3CHO,B中含有官能团为羟基、羧基,答案为:CH3CHO,羟基、羧基;(2)C转化为D的反应类型是取代反应,答案为:取代反应;(3)1molD最多可以和3molNaOH反应,反应的化学方程式为:
 ;
;
(4)E中可以与氢气发生加成反应的有苯环上的不饱和键和一个碳碳双键,所以1molE最多可与4molH2加成,答案为:4;(5)B为 ,能满足如下条件A.能发生银镜反应,含有醛基,B.核磁共振氢谱只有4个峰,即有4组不同环境的氢原子,C.能与FeCl3溶液发生显色反应,有酚羟基,水解时1mol可消耗3molNaOH,含有酯基,综上所述,该物质应该为甲酸苯酚酯,结合核磁共振氢普,写出结构简式为:
,能满足如下条件A.能发生银镜反应,含有醛基,B.核磁共振氢谱只有4个峰,即有4组不同环境的氢原子,C.能与FeCl3溶液发生显色反应,有酚羟基,水解时1mol可消耗3molNaOH,含有酯基,综上所述,该物质应该为甲酸苯酚酯,结合核磁共振氢普,写出结构简式为: ,答案为:
,答案为: ;甲苯可以被酸性高锰酸钾氧化为苯甲酸,所以苯甲酸由甲苯氧化得到,由于酚羟基一般不易直接与羧酸酯化,所以可以根据题目中的乙酰氯制备D的方法来制备本甲酸苯酚酯,即把苯甲酸转化为苯甲酰氯,苯酚由苯经氯气,Fe3+做催化剂取代,在水解得到,经上述反应流程为:
;甲苯可以被酸性高锰酸钾氧化为苯甲酸,所以苯甲酸由甲苯氧化得到,由于酚羟基一般不易直接与羧酸酯化,所以可以根据题目中的乙酰氯制备D的方法来制备本甲酸苯酚酯,即把苯甲酸转化为苯甲酰氯,苯酚由苯经氯气,Fe3+做催化剂取代,在水解得到,经上述反应流程为: .
.

【题目】表是A、B、C、D、E五种有机物的有关信息:
A | B | C | D | E |
①能使溴水褪色 | ①由C、H两 | ①由C、H、O三种元素组成 | ①相对分子质量 | ①由C、H、O三种元素组成 |
根据表中信息回答下列问题:
(1)A与水在一定条件下反应生成的物质C是(填名称);写出在一定条件下,A生成高分子化合物的化学方程式: .
(2)A与氢气发生加成反应后生成分子F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式 . 当n=时,这类有机物开始出现同分异构体.
(3)B具有的性质是(填序号). ①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤任何条件下不与氢气反应 ⑥可使酸性高锰酸钾溶液和溴水均褪色
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式: .
(4)写出由C氧化生成D的化学方程式: .
(5)C与E反应能生成相对分子质量为100的酯,该反应类型为;其化学方程式为: .
【题目】有三份白色固体分别为碳酸钠、碳酸氢钠及二者的混合物。某化学课外活动小组对其进行相关实验和探究。
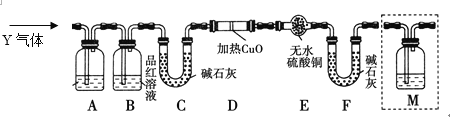
I.甲组同学采用加热的方法确定其成分。
(1)除托盘天平、药匙、三脚架、泥三角、玻璃棒和干燥器外,完成本实验还需要的实验仪器有_________。
(2)该小组同学准确称取一定量的样品m1g,多次加热、冷却、称量直至恒重,质量为m2g。依据得出结论,请完成下表。
m2与m1的关系 | 结论 | |
① | 样品为Na2CO3 | |
② | 样品为NaHCO3 | |
③ | 样品为Na2CO3和 NaHCO3的混合物 |
II.乙组同学利用已鉴别出的NaHCO3和Na2CO3,继续进行实验,对于“能否用CaCl2鉴别的NaHCO3和Na2CO3”的问题进行探究。
(3)小组同学先将NaHCO3、Na2CO3、CaCl2固体分别配制成0.5mol/L的溶液。设汁如下实验方案:
表1
实验方案 | 预测现象 | |
实验1 | 向2mL Na2CO3溶液中滴加1mL CaCl2溶液 | 有白色沉淀生成 |
实验2 | 向2mL NaHCO3溶液中滴加1mL CaCl2溶液 | 无白色沉淀生成 |
若已知:①室温下,0.5mol/L NaHCO3溶液pH=8.5,溶液中c(HCO3-)=0.49 mol/L 。
②室温下, H2CO3的二级电离常数K2=5.6×10-11。
③Ksp(CaCO3)=2.8×10-9。
试估算使0.5mol/L NaHCO3溶液中的CO32-沉淀所需的c(Ca2+)应不低于_____mol/L,并由此得出结论:实验2的预测现象_____(填“正确”或“不正确”)。
⑷实际实验过程发现实验2的现象为白色沉淀并有无色气体生成。此现象对应的离子方程式为_____________。
(5)该小组同学继续设计实验对NaHCO3溶液与CaCl2溶液的反应进行探究,利用气体压力传感器得到的部分实验数据如下:(注:CaCl2溶液浓度相同)
表2 容器内气体浓度达到10000ppm所需时间
C(NaHCO3)/(mol/L) | 所需时间/s | |||
v(CaCl2):v(NaHCO3) | ||||
1:5 | 2:5 | 4:5 | 1:1 | |
1.0 | 142 | 124 | 114 | 156 |
0.5 | 368 | 264 | 244 | 284 |
0.25 | 882 | 450 | 354 | 632 |
0.1 | 1126 | 1316 | 816 | 1816 |
由实验数据可得出的结论是:
①当v(CaCl2):v(NaHCO3)一定时,随着_____,气体逸出速率减小;
②NaHCO3浓度在0.1~1.0mol/L,v(CaCl2)与v(NaHCO3)的比值为____时,气体逸出速率最快,可获得理想的实验观察效果。