题目内容
关于小苏打水溶液的表述正确的是( )
分析:A.从物料守恒的角度分析;
B.根据溶液的电中性原则分析;
C.NaHCO3溶液呈碱性,HCO3-的水解大于CO32-的电离;
D.溶液存在NaHCO3和H2O,结合电解质的强弱判断.
B.根据溶液的电中性原则分析;
C.NaHCO3溶液呈碱性,HCO3-的水解大于CO32-的电离;
D.溶液存在NaHCO3和H2O,结合电解质的强弱判断.
解答:解:A.小苏打为NaHCO3,根据物料守恒可知,溶液中存在c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3),故A错误;
B.溶液存在电荷守恒:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故B错误;
C.NaHCO3溶液呈碱性,HCO3-的水解大于CO32-的电离,故C错误;
D.溶液存在NaHCO3和H2O,为强电解质,完全电离:NaHCO3=Na++HCO3-,HCO3-存在电离平衡:HCO3-?H++CO32-,还存在H2O?H++OH-,故D正确.
故选D.
B.溶液存在电荷守恒:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故B错误;
C.NaHCO3溶液呈碱性,HCO3-的水解大于CO32-的电离,故C错误;
D.溶液存在NaHCO3和H2O,为强电解质,完全电离:NaHCO3=Na++HCO3-,HCO3-存在电离平衡:HCO3-?H++CO32-,还存在H2O?H++OH-,故D正确.
故选D.
点评:本题考查离子浓度的大小比较,题目难度中等,注意结合物料守恒、电荷守恒的角度分析,特别NaHCO3溶液呈碱性的特点,为解答该题的关键.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
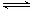 H++CO32—
H++CO32—