题目内容
18.下列说法不正确的是( )| A. | 1 mol 氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4 L | |
| B. | 1 mol臭氧和1.5 mol氧气含有相同的氧原子数 | |
| C. | 等体积、浓度均为1 mol•L-1的磷酸和盐酸,H3PO4和HCl含有的氢元素质量之比为1:1 | |
| D. | 等物质的量的干冰和葡萄糖(C6H12O6)中所含碳原子数之比为1:6,氧原子数之比为1:3 |
分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$=$\frac{V}{{V}_{m}}$=cV结合物质的构成计算.
解答 解:A.n(O)=$\frac{12.04×1{0}^{23}}{6.02×1{0}^{23}/mol}$=2mol,则n(O2)=1mol,体积为22.4L,故A正确;
B.1 mol臭氧和1.5 mol氧气都含有3molO原子,数目相同,故B正确;
C.等体积、浓度均为1 mol•L-1的磷酸和盐酸,H3PO4和HCl的物质的量相等,则含有的氢元素质量之比为3:1,故C错误;
D.由化学式可知等物质的量的干冰和葡萄糖(C6H12O6)中所含碳原子数之比为1:6,氧原子数之比为1:3,故D正确.
故选C.
点评 本题综合考查物质的量的相关计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握物质的构成特点,难度中等.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
9.SO2的含量是空气质量日报中一项重要检测指标,请结合所学知识回答下列问题.
(1)工业制硫酸过程中,SO2催化氧化的原理为:
2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g)
T℃时,向某密闭容器中充入一定SO2(g)和O2(g),发生上述反应,测得SO2(g)的平衡转化率(a)与体系总压强(p)的关系如图1所示.
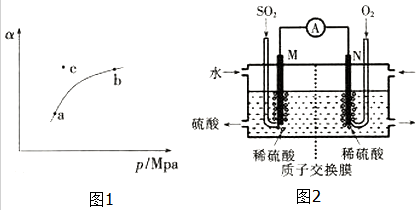
①a、b两点对应的平衡常数K(a)=K(b)(填“>”、“<”或“=”,下同),SO2浓度c(a)>c(b).
②c点时,反应速率v(正)<v(逆).
(2)电化学法处理SO2.
硫酸工业尾气中的SO2经分离后,可用于制备硫酸,同时获得电能,装置如图2所示(电极均为惰性材料):
①M极发生的电极反应式为SO2-2e-+2H2O=4H++SO42-.
②若使该装置的电流强度达到2.0A,理论上每分钟应向负极通入标准状况下气体的体积为0.014L(已知:1个e-所带电量为1.6×10-19C).
(3)溶液法处理SO2.
已知常温下H2SO3和H2CO3的电离常数如表所示:
常温下,将SO2缓慢通入100mL 0.2mol•L-1的Na2CO3溶液中,当通入448mLSO2时(已折算为标准状况下的体积,下同),发生的离子方程式为SO2+H2O+CO32-=HCO3-+HSO3-;当通入896mLSO2时,所得溶液呈弱酸性,溶液中各离子浓度由大到小的顺序为c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-).
(1)工业制硫酸过程中,SO2催化氧化的原理为:
2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g)
T℃时,向某密闭容器中充入一定SO2(g)和O2(g),发生上述反应,测得SO2(g)的平衡转化率(a)与体系总压强(p)的关系如图1所示.

①a、b两点对应的平衡常数K(a)=K(b)(填“>”、“<”或“=”,下同),SO2浓度c(a)>c(b).
②c点时,反应速率v(正)<v(逆).
(2)电化学法处理SO2.
硫酸工业尾气中的SO2经分离后,可用于制备硫酸,同时获得电能,装置如图2所示(电极均为惰性材料):
①M极发生的电极反应式为SO2-2e-+2H2O=4H++SO42-.
②若使该装置的电流强度达到2.0A,理论上每分钟应向负极通入标准状况下气体的体积为0.014L(已知:1个e-所带电量为1.6×10-19C).
(3)溶液法处理SO2.
已知常温下H2SO3和H2CO3的电离常数如表所示:
| 电离常数 酸 | K1 | K2 |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
3.某氯原子的质量为a g,12C原子的质量为b g,用NA表示阿伏加德罗常数.下列说法中不正确的是( )
| A. | 由该氯原子构成氯分子(Cl2)的相对分子质量为$\frac{24a}{b}$ | |
| B. | mg该氯原子的物质的量为$\frac{m}{aNA}$ mol | |
| C. | ng该氯原子所含的电子数为$\frac{17n}{aNA}$ | |
| D. | 1mol该氯原子的质量为aNA g |
10.下列关于有机化合物的说法正确的是( )
| A. | 苯在常温下可与溴水发生取代反应 | |
| B. | 葡萄糖能发生氧化反应和银镜反应 | |
| C. | 乙醇和乙酸都能与氢氧化钠反应 | |
| D. | 糖类、油脂和蛋白质都能发生水解反应 |
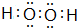 ;试用电子式表示原子个数比为2:1的该化合物的形成过程
;试用电子式表示原子个数比为2:1的该化合物的形成过程 .
.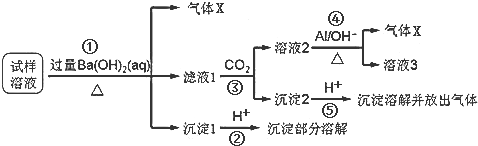
 某兴趣小组同学研究了氧族元素及其某些化合物的部分性质,查阅资料如下:
某兴趣小组同学研究了氧族元素及其某些化合物的部分性质,查阅资料如下: