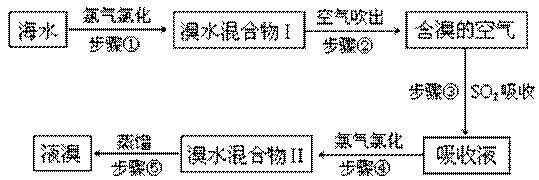
题目内容
将6.4g铜和足量浓硝酸反应,Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
(1)有多少摩尔硝酸被还原?
(2)产生的二氧化氮在标准状况下的体积是多少升?
(1)有多少摩尔硝酸被还原?
(2)产生的二氧化氮在标准状况下的体积是多少升?
(1)6.4g铜全部被氧化,提供电子的物质的量=
mol×2=0.2mol,而硝酸中+5价的N被还原成二氧化氮中+4价的N,需要得到1mol电子,所以要得到0.2mol得电子,只能还原0.2mol硝酸,答:有0.2mol硝酸被还原;
(2)铜和二氧化氮的关系式为:Cu----2NO2,铜的物质的量=
mol=0.1mol,根据关系式知,0.1mol铜与硝酸反应可以得到0.2mol二氧化氮,二氧化氮在标况下的体积=0.2mol×22.4L/mol=4.48L,答:二氧化氮的体积是4.48L.
| 6.4 |
| 64 |
(2)铜和二氧化氮的关系式为:Cu----2NO2,铜的物质的量=
| 6.4 |
| 64 |

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目