题目内容
2.下列判断或叙述正确的是( )| A. | 盛装NaOH溶液的试剂瓶用橡胶塞,不用玻璃塞 | |
| B. | 水晶是无色透明的晶体,可以制成硅太阳能电池 | |
| C. | 将FeCl3饱和溶液滴入沸水中,可以立即得到Fe(OH)3胶体 | |
| D. | 铝箔在空气中受热可以熔化,剧烈燃烧,产生大量的热 |
分析 A.试剂瓶为玻璃仪器,玻璃中含有二氧化硅,能与碱性溶液反应生成硅酸钠;
B.水晶是二氧化硅晶体,制作硅太阳能电池的原料为晶体硅;
C.缺少继续加热至液体呈红褐色位置这一步骤;
D.铝箔受热时表面的氧化铝兜着熔化的铝,阻止了铝与氧气的进一步反应.
解答 解:A.玻璃中的二氧化硅与氢氧化钠溶液反应生成具有较强黏性的硅酸钠溶液,时间长了就打不开了,因此盛放碱性溶液的试剂瓶用橡胶塞,故A正确;
B.水晶是无色透明的石英晶体,制作硅太阳能电池的原料为晶体硅而非二氧化硅晶体,故B错误;
C.氢氧化铁胶体的制备方法为:将FeCl3饱和溶液滴入沸水中,继续加热至液体呈红褐色,停止加热,故C错误;
D.铝箔受热时表面生成一层致密的氧化铝薄膜,氧化铝的熔点比Al的高,兜着熔化的铝,阻止了铝与氧气的进一步反应,故D错误;
故选A.
点评 本题考查非金属元素及其化合物的知识,涉及硅单质及二氧化硅的应用,氢氧化铁胶体的制备、铝的性质,难度不大,其中石英晶体和晶体硅的应用容易混淆.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.常温下,0.01mol/L的盐酸与pH=12的NaOH溶液按体积比9:1混合,混合后溶液的pH为( )
| A. | 7 | B. | 2.1 | C. | 2.3 | D. | 11.9 |
10.关于硅及其化合物的叙述错误的是( )
| A. | SiO2是生产粗硅的主要原料 | |
| B. | 晶体硅(Si)是生产光缆和光导纤维的主要原料 | |
| C. | 水泥、玻璃、陶瓷的主要成份都是硅酸盐 | |
| D. | 盛放氢氧化钠溶液的玻璃试剂瓶不能用磨口玻璃塞 |
17.下列离子方程式正确的是( )
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 向NaAlO2溶液中通过量CO2:AlO2-+CO2+H2O═Al(OH)3↓+CO32- | |
| C. | 电路板腐蚀液中的反应:Cu+2Fe3+═2Fe2++Cu2+ | |
| D. | 小苏打溶液与NaOH溶液混合:HCO3-+OH-═CO2↑+H2O |
14.下列离子能大量共存于同一溶液中的是( )
| A. | HCO3-、OHˉ、K+、Clˉ | B. | Al3+、H+、Clˉ、K+ | ||
| C. | SO42-、Na+、OHˉ、K+ | D. | Fe2+、K+、OHˉ、Clˉ |
11.有机物香茅醇的结构简式为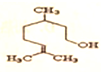 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 化学式为C10H20O | B. | 遇FeCl3溶液发生显色反应 | ||
| C. | 属于芳香族化合物 | D. | 该有机物易溶于水 |
12.某课外实验小组设计的下列实验不合理的是( )
| A. | 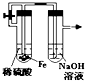 制备并观察氢氧化亚铁 | B. | 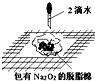 证明过氧化钠与水反应放热 | ||
| C. | 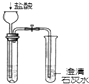 鉴别碳酸钠与亚硫酸钠 | D. | 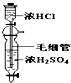 制备少量干燥的氯化氢气体 |
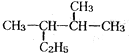
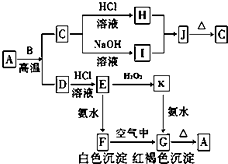 A是一种红棕色金属氧化物,B、D是常见金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解.
A是一种红棕色金属氧化物,B、D是常见金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解.