题目内容
【题目】苯甲酸甲酯是一种重要的工业原料,某研究性学习小组的同学拟用下列装置制取高纯度的苯甲酸甲酯。
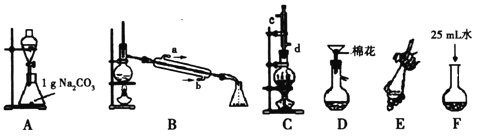
有关数据如下表:
熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 水溶性 | |
苯甲酸 | 122.4 | 249 | 1.27 | 微溶 |
甲醇 | -97 | 64.3 | 0.79 | 互溶 |
苯甲酸甲酯 | -12.3 | 199.6 | 1.09 | 不溶 |
(1)在烧瓶中混合有机物及浓硫酸的方法是__________________________________,在实际实验中,甲醇、苯甲酸的物质的量之比远大于理论上物质的量之比,目的是_______________。装置C中除甲醇、苯甲酸与浓硫酸外还需要放置____________________________。
(2)B装置需加热的玻璃仪器的名称__________,C装置上部的冷凝管的主要作用是_____________________。冷却剂在冷凝管中的流动方向是__________。
(3)制备和提纯苯甲酸甲酯的操作先后顺序为(填装置字母代号)________________。
(4)A中Na2CO3的作用是_____________________;D装置的作用是_______________;当B装置中温度计显示_____________℃时可收集苯甲酸甲酯。
【答案】 先将一定量的苯甲酸放入烧瓶中,然后再加入甲醇,最后边振荡边缓慢加入一定量的浓硫酸 提高苯甲酸的利用率 沸石或碎瓷片 蒸馏烧瓶 冷凝回流、导气 从d口进、C口流出 CFEADB 除去酯中的苯甲酸 除未反应完的Na2CO3 199.6
【解析】(1)参考浓硫酸的稀释,先将一定量的苯甲酸放入烧瓶中,然后再加入甲醇,最后边振荡边缓慢加入一定量的浓硫酸来配制混合液,通过增加甲醇的量,提高苯甲酸的转化率,给液体混合物加热时通常添加沸石防暴沸;
(2)B装置需加热的玻璃仪器的名称为蒸馏烧瓶,C装置上部的冷凝管可使反应混合加热时挥发出的蒸汽经冷凝重新回流反应容器中,减少原料的损耗,冷却水的水流方向与蒸汽的流向相反,选择从d口进入,c口流出;
(3)在圆底烧瓶中加入0.1mol苯甲酸和0.4mol甲醇,再小心加入3mL浓硫酸,混匀后,投入几粒沸石,小心加热使反应完全,得苯甲酸甲酯粗产品;苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,需进行分液、蒸馏等操作,可用分液的方法除去苯甲酸甲酯中的硫酸、苯甲酸,然后进行蒸馏,操作的顺序为CFEADB;
(4)碳酸钠用于洗去苯甲酸甲酯中过量的酸,过量的碳酸钠用过滤的方法可除去,蒸馏时,将苯甲酸甲酯与甲醇、水分离,由苯甲酸甲酯的沸点可知应收集沸点199.6℃的馏分,故应控制温度199.6℃。

