题目内容
某校化学小组的同学开展K2CO3和NaCl的固体混合物中K2CO3的检验与质量分数测定的探究实验,他们提出下列实验方案。
(一)补全以下检验混合物中存在K2CO3的实验步骤及相关现象
(1)取混合物样品溶于水,分别取少量溶液进行以下实验
(2)_________________________________________则一定存在K+;
(3)___________________________________________________则一定存在CO32—。
(二)测定K2CO3质量分数
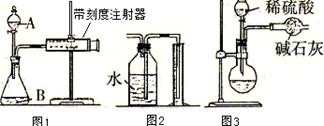
(1)甲同学用图1所示装置,把xg的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积。实验开始时检查该装置气密性的方法是 。
(2)乙同学用图2代替图1中的收集装置,则所测K2CO3质量分数 (填“偏大”、“偏小”、“不变”),你的改进方案是 。
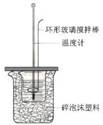
(3)丙同学用图3装置测定CO2的质量,该装置存在较多缺陷,从而导致实验误差,请你填写其中的三点缺陷:I ;Ⅱ ;Ⅲ
(一)补全以下检验混合物中存在K2CO3的实验步骤及相关现象
(1)取混合物样品溶于水,分别取少量溶液进行以下实验
(2)_________________________________________则一定存在K+;
(3)___________________________________________________则一定存在CO32—。
(二)测定K2CO3质量分数

(1)甲同学用图1所示装置,把xg的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积。实验开始时检查该装置气密性的方法是 。
(2)乙同学用图2代替图1中的收集装置,则所测K2CO3质量分数 (填“偏大”、“偏小”、“不变”),你的改进方案是 。
(3)丙同学用图3装置测定CO2的质量,该装置存在较多缺陷,从而导致实验误差,请你填写其中的三点缺陷:I ;Ⅱ ;Ⅲ
(一)2.用焰色反应,同时透过钴玻璃片观看燃烧的火焰,如果是紫色的;
3.加入氯化钡溶液有白色沉淀,再加入盐酸沉淀溶解生成无色无味使澄清石灰水浑浊的气体。
(二)(1)关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位;
(2)偏小;将水换成饱和碳酸氢钠溶液;
(3):①产生的CO2气体中混有水蒸气,同时被碱石灰吸收,导致结果偏大;②反应结束后装置内残留的CO2气体不能全部排出,导致结果偏小;③球形干燥管与空气相通,也会吸收空气中的CO2和水蒸气,导致结果偏大;④实验开始时,装置内的空气中会有部分CO2也会被碱石灰吸收,导致结果偏大等。.
3.加入氯化钡溶液有白色沉淀,再加入盐酸沉淀溶解生成无色无味使澄清石灰水浑浊的气体。
(二)(1)关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位;
(2)偏小;将水换成饱和碳酸氢钠溶液;
(3):①产生的CO2气体中混有水蒸气,同时被碱石灰吸收,导致结果偏大;②反应结束后装置内残留的CO2气体不能全部排出,导致结果偏小;③球形干燥管与空气相通,也会吸收空气中的CO2和水蒸气,导致结果偏大;④实验开始时,装置内的空气中会有部分CO2也会被碱石灰吸收,导致结果偏大等。.
(一)钾离子的检验一般用焰色反应,即用焰色反应,同时透过钴玻璃片观看燃烧的火焰,如果是紫色的,说明含有钾离子;CO32-的检验可以氯化钡和盐酸,即加入氯化钡溶液有白色沉淀,再加入盐酸沉淀溶解生成无色无味使澄清石灰水浑浊的气体。
(二)(1)由于有注射器,所以检查该装置气密性的方法是关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位;
(2)由于CO2能溶于水,造成收集的CO2体积减少,所以测定结果偏小;改正的方法是减少CO2的溶解,所以可将水换成饱和碳酸氢钠溶液。
(3)考查实验的评价,根据实验装置图即原理可知,存在的问题是①产生的CO2气体中混有水蒸气,同时被碱石灰吸收,导致结果偏大;②反应结束后装置内残留的CO2气体不能全部排出,导致结果偏小;③球形干燥管与空气相通,也会吸收空气中的CO2和水蒸气,导致结果偏大;④实验开始时,装置内的空气中会有部分CO2也会被碱石灰吸收,导致结果偏大等。
(二)(1)由于有注射器,所以检查该装置气密性的方法是关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位;
(2)由于CO2能溶于水,造成收集的CO2体积减少,所以测定结果偏小;改正的方法是减少CO2的溶解,所以可将水换成饱和碳酸氢钠溶液。
(3)考查实验的评价,根据实验装置图即原理可知,存在的问题是①产生的CO2气体中混有水蒸气,同时被碱石灰吸收,导致结果偏大;②反应结束后装置内残留的CO2气体不能全部排出,导致结果偏小;③球形干燥管与空气相通,也会吸收空气中的CO2和水蒸气,导致结果偏大;④实验开始时,装置内的空气中会有部分CO2也会被碱石灰吸收,导致结果偏大等。

练习册系列答案
相关题目