题目内容
【题目】有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20,其中C、E是金属元素;A和E属同一族,且A为非金属元素,它们原子的最外层电子排布为ns1,B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)A是________,B是________,E是________(写元素符号)。
(2)写出C元素基态原子的电子排布式__________________________________。
(3)用轨道表示式表示D元素原子的价电子排布__________________________。
【答案】 H O K 1s22s22p63s23p1 
【解析】A、B、C、D、E5种短周期元素,它们的核电荷数依次增大,且都小于20,B和D属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,最外层电子排布为ns2np4,则B为O元素、D为S元素;A和E属同一族,它们原子的最外层电子排布为ns1,处于IA族,E的原子序数大于硫,且5种元素中只有C、E是金属元素,则A为H元素、E为K元素;C原子最外层上电子数等于D原子最外层上电子数的一半,其最外层电子数为6×![]() =3,故C为Al。
=3,故C为Al。
(1)由上述分析可知,A为H、B为O、C为K,故答案为:H;O;K;
(2)C为铝元素元素,原子核外有13个电子,基态原子的电子排布为1s22s22p63s23p1 或[Ne]3s23p1,故答案为:1s22s22p63s23p1 或[Ne]3s23p1;
(3)D为S元素,原子价层电子排布为3s23p4,轨道表示式为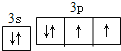 ,故答案为:
,故答案为: 。
。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目