题目内容
【题目】某含铜样品的主要成分为a CuCO3·bCu(OH)2(a、b均为最简正整数)。为测定其化学组成和Cu元素的质量分数。甲乙两个实验小组查阅资料,设计了不同的实验方案(假定杂质对实验无干扰)。
Ⅰ.甲组同学利用一下方法测定:
①在一定质量的样品中加入过量的稀硫酸,过滤,测量产生气体的体积
②在滤液中加过量的NaOH稀溶液,过滤
③灼烧②中所得滤渣、直至残留固体恒重
(1)为了除去滤渣中的可溶性杂质,需要对滤渣进行的操作是_____,滤渣应在_____(填仪器名称)中进行灼烧。
(2)利用右图装置测量气体体积,读数时应注意:
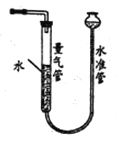
①恢复至室温;②__________;③平视且视线与凹液面最低点相切。
若操作无误,但气体体积测量结果仍然明显偏低,合理的改进措施是____________。
(3)甲组同学在处理实验数据时,将常温常压下测得的气体体积VL换算成V/22.4mol进行计算,则计算所得a值将_______(填“偏大”、“偏小”或“无影响”)。
Ⅱ.乙组同学利用下图装置进行测量(夹持及加热装置略去):
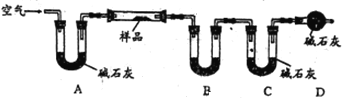
(4)U型管B中的药品是_________,D的作用是_________。
(5)若样品的质量为20g,充分反应后测得B中固体质量增加了0.9g,C中固体质量增加了4.4g,则样品中主要成分的化学式为___________,样品中铜元素的质量分数为____________。
【答案】 洗涤 坩埚 调节量气管和水准管的液面相平 将量气装置中的水换为饱和碳酸氢钠溶液(答案合理即可) 偏大 无水氯化钙(合理即可) 防止空气中的水蒸气和二氧化碳进入装置C,影响测定结果 2CuCO3·Cu(OH)2 48%
【解析】(1)为了除去滤渣中的可溶性杂质,需要对滤渣进行的操作是洗涤,固体应在坩埚中进行灼烧。(2)由于气体体积受压强影响较大,因此读数时应注意:①恢复至室温;②调节量气管和水准管的液面相平 ;③平视且视线与凹液面最低点相切。由于CO2能溶于水,所以需要尽可能减少溶解,改进措施是将量气装置中的水换为饱和碳酸氢钠溶液;(3)常温常压下气体的摩尔体积大于22.4L/mol,因此测得的气体体积VL换算成V/22.4mol进行计算,则计算所得a值将偏大。(4)样品分解产生CO2、水蒸气,所以U型管B中的药品是 无水氯化钙,用来吸收水蒸气。C中碱石灰用来吸收CO2。由于空气中还含有水蒸气和CO2,所以D中碱石灰的作用是防止空气中的水蒸气和二氧化碳进入装置C,影响测定结果。(5)充分反应后测得B中固体质量增加了0.9g,水的物质的量是0.9g÷18g/mol=0.05mol。C中固体质量增加了4.4g,CO2的物质的量是4.4g÷44g/mol=0.1mol,所以a:b=0.1:0.05=2:1,则样品中主要成分的化学式为2CuCO3·Cu(OH)2,样品中铜元素的质量分数为![]() 。
。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案