题目内容
【题目】目前工业上有一种方法是用CO2生产燃料甲醇(CH3OH)。一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。
CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ·mol—1)的变化。
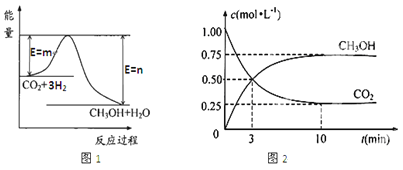
(1)该反应为_________热反应,原因是_____________________。
(2)下列能说明该反应已经达到平衡状态的是_________(填序号)
A.v (H2)=3v(CO2) B.容器内气体压强保持不变
C.v逆(CO2)=v正(CH3OH) D.容器内气体密度保持不变
E.CH3OH 中1 mol H—O键断裂的同时2 mol C=O键断裂
F. 混合气体的平均摩尔质量不变
(3)在体积为1 L的密闭容器中,充入1 molCO2和3 molH2,测得CO2和CH3OH(g)的浓度随时间变化如图2所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率v (H2)=________。 达平衡时容器内平衡时与起始时的压强比____________。
(4)甲醇、氧气在酸性条件下可构成燃料电池,其负极的电极反应为________________,
与铅蓄电池相比,当消耗相同质量的负极物质时,甲醇燃料电池的理论放电量是铅蓄电池的___________倍(保留小数点后1位)。
【答案】 放热 生成物的能量低于反应物的能量 BCEF 0.225 5:8 CH3OH-6e-+H2O=6H++CO2 19.4
【解析】(1)由图可知,反应物的总能量大于生成物的总能量,则该反应为放热反应;(2)A.v (H2)= 3v(CO2) ,始终存在,不能判断正逆反应速率关系,不能判定平衡状态,A错误;B.该反应为气体体积不等的反应,则容器内气体压强保持不变,达到平衡状态,B正确;C.v逆(CO2)= v正(CH3OH) ,可知正逆反应速率相等,能判定平衡状态,C正确;D.混合气体的质量、体积不变,则容器内气体密度始终保持不变,不能判定平衡状态,D错误;E.1mol H-O键断裂的同时2mol C=O键断裂,可知正逆反应速率相等,能判定平衡状态,E正确;F.混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量不变,但物质的量是变化的,所以混合气体的平均摩尔质量不变说明反应达到平衡状态,F正确;答案选BCEF;(3)CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
开始 1 3 0 0
转化 0.75 2.25 0.75 0.75
平衡 0.25 0.75 0.75 0.75
从反应开始到平衡,用氢气浓度变化表示的平均反应速率v (H2)=2.25mol/L÷10min=0.225mol/(L·min);达平衡时容器内平衡时与起始时的压强之比为(0.25+0.75+0.75+0.75):(1+3)=5:8;
(4)甲醇、氧气在酸性条件下可构成燃料电池,其负极的电极反应式为CH3OH-6e-+H2O=6H++CO2;铅蓄电池中负极材料为Pb,氧化为PbSO4,甲醇燃料电池中负极通入甲醇,氧化生成CO2,相同质量提供电子数目之比为![]() =32:621,则甲醇燃料电池的理论放电量是铅蓄电池的621/32=19.4倍。
=32:621,则甲醇燃料电池的理论放电量是铅蓄电池的621/32=19.4倍。

 53随堂测系列答案
53随堂测系列答案【题目】一定条件下进行反应:COCl2(g) ![]() Cl2(g)+CO(g),向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),反应过程中测得的有关数据见下表:
Cl2(g)+CO(g),向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),反应过程中测得的有关数据见下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
下列说法不正确的是( )
A. 使用恰当的催化剂能加快该反应速率
B. 该条件下,COCl2的最大转化率为60%
C. 6s时,反应达到最大限度即化学平衡状态
D. 生成Cl2的平均反应速率,0~2s比2~4s快
【题目】甲醇是一种重要的有机化工原料。
(1)已知:
①C2H4(g)+H2O(g) ![]() C2H5OH(g) ΔH1=-45.5kJ/mol
C2H5OH(g) ΔH1=-45.5kJ/mol
②2CH3OH(g) ![]() CH3OCH3(g)+H2O(g) ΔH2=-23.9kJ/mol
CH3OCH3(g)+H2O(g) ΔH2=-23.9kJ/mol
③C2H4OH(g) ![]() CH3OCH3(g) ΔH3=+50.7kJ/mol
CH3OCH3(g) ΔH3=+50.7kJ/mol
请写出乙烯和水蒸气化合生成甲醇气体的热化学方程式:_____________。
(2)合成甲醇的反应为:CO(g)+2H2(g) ![]() CH3OH(g) ΔH。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图甲所示。
CH3OH(g) ΔH。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图甲所示。

①温度升高甲醇的体积分数增大的原因是___________;
②根据图像判断ΔH________________(填“>”、“<”或“=”)0。
(3)某研究小组提出将4CH3OH+6NO2+8OH-=3N2+4CO32-+12H2O设计成原电池,以实现污染物的利用,装置如图乙所示(图中电极均为多孔的惰性电极)。

①电极A的名称是_____________。
②写出原电池电极B的电极反应式:___________。
③若用该电池对铁制品表面镀铜,反应一段时间后,铁制品质量增加64g,理论上处理NO2的质量为________g。
(4)为了研究甲醇转化为二甲醚的反应条件,某研究与小组在三个体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ΔH2=-23.9KJ/mol。
CH3OCH3(g)+H2O(g) ΔH2=-23.9KJ/mol。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
Ⅰ | T1 | 0.20 | 0.080 | 0.080 |
Ⅱ | T1 | 0.40 | a | a |
Ⅲ | T2 | 0.20 | 0.090 | 0.090 |
①T1温度下该反应的平衡常数K=_______;反应温度T1_________T2(填“大于”或“小于”。)
②容器Ⅱ中a=______。
③下列说法能说明反应达到平衡状态的是___________(填字母)。
A.容器中气体压强不再变化
B.用CH3OH 和CH3OCH3表示的反应速率之比为2:1
C.混合气体的密度不变
D.容器内CH3OH和CH3OCH3的浓度之比为2:1
E.单位时间内生成2molCH3OH 的同时生成1mol H2O(g)