��Ŀ����
����Ŀ��36.5 g HCl�����ܽ���1 Lˮ��(ˮ���ܶ�Ϊ1 g��cm��3)��������Һ���ܶ�Ϊ�� g��cm��3����������Ϊw�����ʵ���Ũ��Ϊc��NA��ʾ�����ӵ���������ֵ��������������ȷ����
A.������Һ�����ʵ���Ũ�ȣ�c��1 mol��L��1B.������Һ�к���NA��HCl����
C.36.5 g HCl����ռ�����Ϊ22.4 LD.������Һ����������������w��![]() ��100%
��100%
���𰸡�D
��������
A��36.5gHCl�ܽ���1Lˮ��(ˮ���ܶȽ���Ϊ1g/ml)��������Һ����Ϊ�Ȼ��⣬���ʵ���Ũ��c=![]() =
=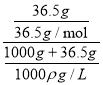 =
=![]() mol/L����A����
mol/L����A����
B���Ȼ�������ˮ�γ�������Һ��ǿ����ʣ���Һ�����Ȼ�����ӣ���B����
C��36.5gHCl�������ʵ���Ϊ1mol����״����ռ�е����Ϊ22.4L��ѡ�����¶�ѹǿ��֪����C����
D������Һ�����Ϊ1L��������Һ��������������=![]() =
=![]() ����D��ȷ��
����D��ȷ��
�ʴ�ΪD��

��ϰ��ϵ�д�
�����Ŀ