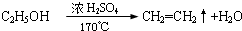
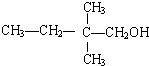
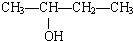题目内容
6.下列说法正确的是( )| A. | 硫酸的摩尔质量为98g | |
| B. | 3.01×1023个SO2分子的质量为32g | |
| C. | 1 mol H2O的质量为18g/mol | |
| D. | 1mol任何物质实际都约含有6.02×1023个原子 |
分析 A.摩尔质量单位错误;
B.根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$计算;
C.根据n=nM计算,质量单位错误;
D.根据1mol任何物质中含有6.02×1023个粒子,进行分析解答.
解答 解:A.硫酸的摩尔质量为98g/mol,故A错误;
B.n(SO2)=$\frac{3.01×1{0}^{23}}{6.02×1{0}^{23}/mol}$=0.5mol,m(SO2)=0.5mol×64g/mol=32g,故B正确;
C.1molH2O的质量n=nM=1mol×18g/mol=18g,故C错误;
D.1mol任何物质中含有6.02×1023个粒子,但1mol任何物质不一定都约含有6.02×1023个原子,由多原子构成的分子,如1mol氢气中含有6.02×1023个×2=12.04×1023个原子,故D错误;
故选B.
点评 本题考查较为综合,涉及物质的量的相关概念和物理量的计算,为高频考点,侧重于学生对概念的理解和计算能力的考查,难度不大.

练习册系列答案
相关题目
16.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 25°C,1.01×105Pa,64gSO2中含有的原子数为3NA | |
| C. | 在常温常压下,11.2LCl2含有的分子数为0.5NA | |
| D. | 标准状况下,11.2LH2O含有的分子数为0.5NA |
17.现有部分短周期元素的性质或原子结构如下表:
①元素X的一种同位素可测定文物年代,这种同位素的符号是 14C.
②T的氢化物一个分子中核外共有18个电子,其结构式为H-S-H;
③Y的氢化物与Y的最高价氧化物的水化物反应生成的物质名称为:硝酸铵
④T与X形成的常见化合物的电子式为: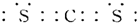 ;
;
⑤Z所在族元素的氢化物中,沸点最低的物质的化学式为:HCl
⑥元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b.
a.常温下Z单质的熔沸点比T单质的熔沸点低
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
d.T元素原子得电子的数目比Z元素原子得电子多.
| 元素编号 | 元素性质或原子结构 |
| T | 最外层电子占核外电子总数的$\frac{3}{8}$ |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
②T的氢化物一个分子中核外共有18个电子,其结构式为H-S-H;
③Y的氢化物与Y的最高价氧化物的水化物反应生成的物质名称为:硝酸铵
④T与X形成的常见化合物的电子式为:
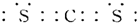 ;
;⑤Z所在族元素的氢化物中,沸点最低的物质的化学式为:HCl
⑥元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b.
a.常温下Z单质的熔沸点比T单质的熔沸点低
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
d.T元素原子得电子的数目比Z元素原子得电子多.
14.25℃时,向10mL 0.01mol/L KOH溶液中滴加0.01mol/L苯酚溶液,混合溶液中粒子浓度关系正确的是( )
| A. | pH>7时,c(C6H5O-)>c(K+)>c(H+)>c(OH-) | |
| B. | V[C6H5OH(aq)]=20mL时,c(C6H5O-)+c(C6H5OH)=2c(K+) | |
| C. | pH<7时,c(K+)>c(C6H5O-)>c(H+)>c(OH-) | |
| D. | V[C6H5OH(aq)]=10mL时,c(K+)=c(C6H5O-)>c(OH-)=c(H+) |
15.合成氨工业有下列生产流程,其先后顺序为( )
①原料气制备 ②氨的合成 ③原料气净化和压缩 ④氨的分离.
①原料气制备 ②氨的合成 ③原料气净化和压缩 ④氨的分离.
| A. | ①②③④ | B. | ①③②④ | C. | ④③②① | D. | ②③④① |
8.同种物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应是( )
| A. | 2NaNO3$\frac{\underline{\;\;△\;\;}}{\;}$2NaNO2+O2↑ | B. | SO2+2H2S═S+2H2O | ||
| C. | 3Cl2+6KOH═5KCl+KClO3+3H2O | D. | NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$N2O↑+2H2O |