题目内容
【题目】汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3= K2O+5Na2O+16N2↑,对于该反应,下列判断正确的是
A. NaN3中氮元素的化合价为-3
B. 氧化剂和还原剂是同一物质
C. 被氧化的氮原子与生成的氮气分子个数之比为15:8
D. 反应过程中若转移1mol电子,则产生2.24L气体(标准状况)
【答案】C
【解析】
10NaN3+2KN03→K20+5Na20+16N2↑中,KN03中N元素由+5价降低为0,NaN3中N元素由-![]() 升高为0;根据得失电子守恒,氧化产物、还原产物的比为15:1;反应中转移10mol电子,生成16molN2,以此来解答。
升高为0;根据得失电子守恒,氧化产物、还原产物的比为15:1;反应中转移10mol电子,生成16molN2,以此来解答。
根据化合价代数和等于0,NaN3中氮元素的化合价为-![]() ,故A错误;KN03中N元素由+5价降低为0,KN03是氧化剂,NaN3中N元素由-
,故A错误;KN03中N元素由+5价降低为0,KN03是氧化剂,NaN3中N元素由-![]() 升高为0,是NaN3还原剂,故B错误;KN03中N元素由+5价降低为0,NaN3中N元素由-
升高为0,是NaN3还原剂,故B错误;KN03中N元素由+5价降低为0,NaN3中N元素由-![]() 升高为0,根据得失电子守恒,氧化产物、还原产物的比为15:1,所以被氧化的氮原子与生成的氮气分子个数之比为15:8,故C正确;根据方程式,转移10mol电子,生成16molN2,若转移1mol电子,则产生35.84L气体(标准状况),故D错误。
升高为0,根据得失电子守恒,氧化产物、还原产物的比为15:1,所以被氧化的氮原子与生成的氮气分子个数之比为15:8,故C正确;根据方程式,转移10mol电子,生成16molN2,若转移1mol电子,则产生35.84L气体(标准状况),故D错误。

【题目】某化学学习小组设计了如下从海带灼烧后的海带灰中提取碘单质的流程:
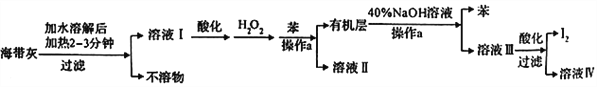
(1)溶解海带灰时要加热煮沸2~3min的目的是_________,操作a的名称是 _______。
(2)向酸化的溶液I中加入H2O2的目的是__________________________________。
(3)已知I2与40%的NaOH溶液反应生成的氧化产物和还原产物的物质的量之比为1:5,则发生反应的化学方程式是________________________________。
(4)最后过滤得到的I2需要进行洗涤和干燥,下列洗涤剂中最应该选用的是______。
a.热水 b.乙醇 c.冷水 d.二硫化碳
(5)用Na2S2O3的标准溶液测定产品的纯度,发生反应:I2+2Na2S2O3=Na2S4O6+2NaI。取5.0g产品,配制成100ml溶液。取10.00ml溶液,以淀粉溶液为指示剂,用浓度为0.050mol·L-1Na2S2O3的标准溶液进行滴定,相关数据记录如下表所示。
编号 | 1 | 2 | 3 |
溶液的体积/mL | 10.00 | 10.00 | 10.00 |
消耗Na2S2O3标准溶液的体积/mL | 19.95 | 17.10 | 20.05 |
滴定时,达到滴定终点的现象是________,碘单质在产品中的质量分数是________% 。