题目内容
3.下列反应的离子方程式正确的是( )| A. | 盐酸与碳酸钠溶液反应:CO32-+2H+=H2O+CO2↑ | |
| B. | 硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ | |
| C. | 碳酸钡溶于醋酸(醋酸是弱酸):BaCO3+2H+=Ba2++H2O+CO2↑ | |
| D. | 金属钠跟水反应:Na+H2O=Na++OH-+H2↑ |
分析 A.反应生成氯化钠、水、二氧化碳;
B.漏写生成氢氧化铜的离子反应;
C.醋酸在离子反应中保留化学式;
D.电子不守恒.
解答 解:A.盐酸与碳酸钠溶液反应的离子反应为CO32-+2H+=H2O+CO2↑,故A正确;
B.硫酸铜溶液与氢氧化钡溶液反应的离子反应为2OH-+Cu2++SO42-+Ba2+═BaSO4↓+Cu(OH)2↓,故B错误;
C.碳酸钡溶于醋酸(醋酸是弱酸)的离子反应为BaCO3+2CH3COOH=Ba2++H2O+CO2↑+2CH3COO-,故C错误;
D.金属钠跟水反应的离子反应为2Na+2H2O=2Na++2OH-+H2↑,故D错误;
故选A.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应方程式书写的方法为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
13.柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾(FeSO4•7H2O)通过下列反应制备:
FeSO4+Na2CO3═FeCO3↓+Na2SO4,FeCO3+C6H8O7═FeC6H6O7+CO2↑+H2O
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
(1)制备FeCO3时,选用的加料方式是c(填字母).
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法取最后一次的洗涤滤液1~2 mL 于试管中,向其中滴加用盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净.
(3)将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80℃下搅拌反应.
①铁粉的作用是防止+2价的铁元素被氧化.
②反应结束后,无需过滤,除去过量铁粉的方法是加入适量柠檬酸让铁粉反应完全.
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得柠檬酸亚铁晶体.分离过程中加入无水乙醇的目的是降低柠檬酸亚铁在水中的溶解量,有利于晶体析出.
(5)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成柠檬酸亚铁.结合图中的绿矾溶解度曲线,完成由烧渣制备绿矾晶体的操作.
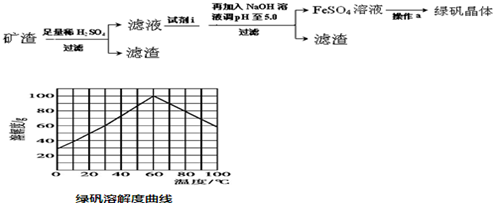
试剂i铁粉,加入试剂i反应的离子方程式为2Fe3++Fe=3Fe2+.操作a为加热到60℃浓缩、冷却结晶、过滤.
FeSO4+Na2CO3═FeCO3↓+Na2SO4,FeCO3+C6H8O7═FeC6H6O7+CO2↑+H2O
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法取最后一次的洗涤滤液1~2 mL 于试管中,向其中滴加用盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净.
(3)将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80℃下搅拌反应.
①铁粉的作用是防止+2价的铁元素被氧化.
②反应结束后,无需过滤,除去过量铁粉的方法是加入适量柠檬酸让铁粉反应完全.
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得柠檬酸亚铁晶体.分离过程中加入无水乙醇的目的是降低柠檬酸亚铁在水中的溶解量,有利于晶体析出.
(5)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成柠檬酸亚铁.结合图中的绿矾溶解度曲线,完成由烧渣制备绿矾晶体的操作.

试剂i铁粉,加入试剂i反应的离子方程式为2Fe3++Fe=3Fe2+.操作a为加热到60℃浓缩、冷却结晶、过滤.
14.不能用离子方程式2H++CO32-=H2O+CO2↑表示的化学方程式是( )
| A. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | B. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ | ||
| C. | K2CO3+2HCl═2KCl+H2O+CO2↑ | D. | Na2CO3+2HNO3═2NaNO3+H2O+CO2↑ |
11.下列离子方程式的书写中,正确的是( )
| A. | 钠跟水反应:Na+2H2O=Na++2OH-+H2↑ | |
| B. | 碳酸氢钠溶液跟盐酸反应:CO32-+2H+=H2O+CO2↑ | |
| C. | 过量二氧化碳跟苛性钾反应:CO2+2OH-=CO32-+H2O | |
| D. | 硫酸氢钾和氢氧化钡按等物质的量在溶液中反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
18.生活中遇到下列问题,不涉及到化学变化的是( )
| A. | 甘油加水作护肤剂 | |
| B. | 蜂、蚁蛰咬处涂抹稀氨水可解痛 | |
| C. | 烹鱼时加入少量的料酒和食醋可减少腥味,增加香味 | |
| D. | 医用酒精可用于皮肤的消毒 |
15.短周期主族元素X、Y、Z、W原子序数依次增大,X-与氦原子电子层结构相同,Y原子核外L层电子数为8且Y与X同主族,Z原子的最外层电子数是内层电子总数的一半,W的最高正价与最低负价的代数和为4,下列说法正确的是( )
| A. | 微粒半径:X<X- | |
| B. | 简单氢化物的稳定性:Z比W的强 | |
| C. | W的氧化物的水化物的酸性一定比Z的强 | |
| D. | 最外层电子数由大到小的顺序为:Z、W、Y |

 .
.