��Ŀ����
����Ŀ������������Ԫ�����ڱ���һ����Ԫ�أ��ش��������⣺
1 | A | |||||||||||||||||
2 | B | |||||||||||||||||
3 | C | D | E | F | G | H | I | |||||||||||
4 | J | K | ||||||||||||||||
5 | ||||||||||||||||||
6 | ||||||||||||||||||
��1����������ĸ�����Ԫ���У���ѧ��������õ�������Ԫ�ط��ű�ʾ����ͬ������ԭ�ӽṹʾ��ͼΪ ��
��2����������ĸ�����Ԫ���У����γ��������������Ԫ��������Ԫ�ط��ű�ʾ����д����Ԫ�صĵ�����C����������ˮ���ﷴӦ�Ļ�ѧ����ʽ ��
��3����C��D��E�γɵ����������У�������ǿ�������û�ѧʽ��ʾ������F��G��H�γɵ��⻯�������ȶ��������û�ѧʽ��ʾ����
��4��A��B���γ�����л��������ṹʽΪ�����Ŀռ乹���� ��
��5����H��K��Ӧ�ĵ����У������Խ����������û�ѧʽ��ʾ����
��6��JԪ���ǹ���Ԫ��������ҵ�ϳ��ó�������Ҫ�ɷ�ΪFe2O3��Ϊԭ�ϣ����ø�¯�����ķ�ʽ��������ԭ���ǣ��ѳ�����̼��ʯ��ʯһ������¯���ڸ����£������ӳ������л�ԭ������д���÷�Ӧ�Ļ�ѧ����ʽ ��
���𰸡�
��1��Ar��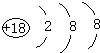
��2��Al��2Al+2NaOH+2H2O=2NaAlO2+3H2��
��3��NaOH��HCl
��4��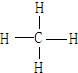 ����������
����������
��5��Br2
��6��Fe2O3+3CO ![]() 2Fe+3CO2
2Fe+3CO2
���������⣺��Ԫ�������ڱ���λ�ã���֪AΪ�⡢BΪ̼��CΪNa��DΪMg��EΪAl��FΪ�ס�GΪ��HΪCl��IΪAr��JΪFe��KΪBr����1��ϡ������Arԭ�������Ϊ�ȶ��ṹ����ѧ��������ã�ԭ�Ӻ��������Ϊ18��ԭ�ӽṹʾ��ͼΪ�� 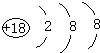 �����Դ��ǣ�Ar��
�����Դ��ǣ�Ar�� 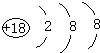 ����2��AlԪ�ص��������敏�����������������������C����������ˮ����ΪNaOH��Al������������Һ��Ӧ����ƫ����������������Ӧ����ʽΪ��2Al+2NaOH+2H2O=2NaAlO2+3H2�������Դ��ǣ�Al��2Al+2NaOH+2H2O=2NaAlO2+3H2������3��������Na��Mg��Al��������������Ӧˮ������NaOH�ļ�����ǿ���ǽ�����ԽǿP��S��Cl���⻯��Խ�ȶ���Ԫ�طǽ�����һ�£���HCl���ȶ������Դ��ǣ�NaOH��HCl����4��A��B���γ�����л�������ΪCH4 �� �ṹʽΪ
����2��AlԪ�ص��������敏�����������������������C����������ˮ����ΪNaOH��Al������������Һ��Ӧ����ƫ����������������Ӧ����ʽΪ��2Al+2NaOH+2H2O=2NaAlO2+3H2�������Դ��ǣ�Al��2Al+2NaOH+2H2O=2NaAlO2+3H2������3��������Na��Mg��Al��������������Ӧˮ������NaOH�ļ�����ǿ���ǽ�����ԽǿP��S��Cl���⻯��Խ�ȶ���Ԫ�طǽ�����һ�£���HCl���ȶ������Դ��ǣ�NaOH��HCl����4��A��B���γ�����л�������ΪCH4 �� �ṹʽΪ  ��Ϊ��������ṹ�����Դ��ǣ�
��Ϊ��������ṹ�����Դ��ǣ�  ���������壻��5���ǽ�����Cl��Br���ǽ�����Խǿ����Ӧ����������Խǿ���������ԣ�Cl2��Br2 �� ���Դ��ǣ�Br2����6����������CO��Ӧ����Fe�������̼����Ӧ����ʽΪ��Fe2O3+3CO
���������壻��5���ǽ�����Cl��Br���ǽ�����Խǿ����Ӧ����������Խǿ���������ԣ�Cl2��Br2 �� ���Դ��ǣ�Br2����6����������CO��Ӧ����Fe�������̼����Ӧ����ʽΪ��Fe2O3+3CO ![]() 2Fe+3CO2 �� ���Դ��ǣ�Fe2O3+3CO
2Fe+3CO2 �� ���Դ��ǣ�Fe2O3+3CO ![]() 2Fe+3CO2 ��
2Fe+3CO2 ��

 �ŵ������ϵ�д�
�ŵ������ϵ�д�