题目内容
(1)刚用小刀切开的金属钠断面呈
(2)切下来的金属钠块要用
(3)金属钠块必须用
(4)金属钠块投入水中后,钠块很快熔成一个闪亮的小球并浮于水面上,这是因为
(5)钠小球在水面上迅速游动,这是因为
(6)如果水中在未加钠之前已滴入酚酞试液,反应后溶液由无色变为
(7)写出钠与水发生的反应方程式
(8)若将金属钠放在空气中加热发生的反应为
| ||
| ||
(2)用滤纸吸干煤油;
(3)钠及其与水反应的产物有腐蚀性;
(4)根据钠的物理性质和钠与水反应放热分析;
(5)钠与水反应生成氢气;
(6)钠与水反应生成氢氧化钠,溶液显碱性;
(7)钠与水反应生成氢氧化钠和氢气;
(8)钠与氧气加热生成过氧化钠.
(2)切下来的金属钠块要用滤纸吸干煤油,故答案为:滤纸;
(3)钠及其与水反应的产物有腐蚀性,而手上会有少量的汗渍,所以直接用手拿,会腐蚀手,应该用镊子,
故答案为:镊子;Na与水反应放出大量热,生成的氢氧化钠具有强腐蚀性;
(4)金属钠块投入水中后,钠与水反应放出大量热,而且钠的熔点较低,密度比水小,所以钠块很快熔成一个闪亮的小球并浮于水面上,
故答案为:反应放热,钠的熔点低,钠的密度比水小;
(5)钠与水反应生成氢气,推动钠四处游动,所以钠小球在水面上迅速游动,这是因为反应生成气体,故答案为:反应生成气体;
(6)钠与水反应生成氢氧化钠,溶液显碱性,所以反应后溶液由无色变为红色,故答案为:红色;Na与水反应生成强碱氢氧化钠;
(7)钠与水反应生成氢氧化钠和氢气,其反应的化学方程式为:2Na+2H2O=2NaOH+H2↑,故答案为:2Na+2H2O=2NaOH+H2↑;
(8)钠与氧气加热生成过氧化钠,其反应的化学方程式为:2Na+O2
| ||
| ||

 阅读快车系列答案
阅读快车系列答案 (13分)过氧化钠(化学式为NaNa2O2)可用在呼吸面具中作为氧气来源。Na2O2能跟CO2反应生成O2和另一种固体化合物(用X表示);它也能跟H2O反应生成O2,化学方程式为:2Na2O2+2H2O = 4NaOH+O2↑。以下是某兴趣小组进行的探究活动。
(1)利用如下图所示实验装置制取氧气,请回答有关问题。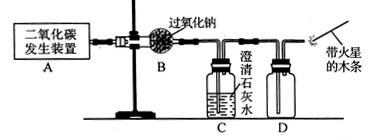
①实验室制取CO2的化学方程式为 。
②表明CO2未被Na2O2完全吸收的实验现象为 。
③O2可采用D装置收集,并用带火星的木条检验,这是利用了O2的 性质。
④若A装置产生的CO2中混有水蒸气,要检验干燥的CO2能否与Na2O2反应生成O2,以上实验装置应如何改进
(2)为探究X是哪种物质及其有关性质,同学们进行了如下分析和实验。
①有同学猜想X可能是酸、碱或盐中的一种。通过对物质组成的分析,大家一致认为X肯定不是酸和碱,理由是 。
②同学们通过讨论和实验证明了X是Na2CO3。以下是他们设计的有关Na2CO3性质的探究实验,将下表填写完整。
| 实验操作 | 现 象 | 有关的化学方程式 |
| 实验一:取少量固体样品, | 澄清石灰水变浑浊 | Na2CO3+2HCl=2NaCl+H2O+CO2↑ CO2+Ca(OH)2=CaCO3↓+H2O |
| 实验二:取少量固体样品, 加水配成溶液,滴加适量的 溶液 | 有白色沉淀产生 | |
某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹).

请按要求填空:
(1)利用B装置可制取的气体有____________(写出两种即可).
(2)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验.
①若在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实
验,实验操作、现象、结论如下:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应的产物具有酸性 |
请你评价实验Ⅰ、Ⅱ的结论是否合理?若不合理,请说明理由________________
________________________________.
②请利用上述装置设计一个简单的实验验证Cl-和Br-的还原性强弱(分别指出甲、乙、丙中盛放的试剂、实验现象及结论)____________
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得并进行NO2有关实验.
①B中发生反应的化学方程式为______________________________________
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹________,再打开止水夹________,使烧杯中的水进入试管丁的操作是________________.
③试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的氧气,直到试管全部充满水,则所得溶液中溶质的物质的量浓度是________(气体按标准状况计算).
(本小题共12分 )某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹).
)某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹).

请按要求填空:
(1)利用B装置可制取的气体有______________________(写出两种即可).
(2)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验.
若在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实
验,实验操作、现象、结论如下:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应的产物具有酸性 |
 电解高铁酸盐(如K2FeO4)是一种高效绿色氧化剂,可用于废水和生活用水的处理.从环境保护的角度看,制备高铁酸盐较好的方法为电解法:Fe+2NaOH+2H2O═Na2FeO4+H2↑.
电解高铁酸盐(如K2FeO4)是一种高效绿色氧化剂,可用于废水和生活用水的处理.从环境保护的角度看,制备高铁酸盐较好的方法为电解法:Fe+2NaOH+2H2O═Na2FeO4+H2↑.

