题目内容
【题目】某研究小组利用BaS的还原性提纯HBr溶液,并制取溴化镁的方案如下:

(1) “还原”步骤中BaS不宜过量太多的原因是______。
(2)滤渣的成分是______。
(3)结晶获得的MgBr2·6H2O用乙醇洗涤,从洗涤液中回收乙醇的实验方法是______。
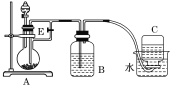
(4)利用如图装置将MgBr2·6H2O脱水得到MgBr2。

①通入HBr的目的是______。
②图中框内装置的作用是______。
(5)已知:BaS+H2O2=Ba(OH)2+S↓。请补充完整实验室由BaS制取高纯BaSO3的实验方案:取BaS加水浸出,边搅拌边在浸出液中加入过量H2O2,过滤,______,(实验中须使用的试剂有:SO2气体,溶有SO2的水,除常用仪器外须使用的仪器有:真空干燥箱、pH计)。
【答案】 后续反应会使用更多的H2SO4、实验过程中会产生有毒的H2S气体 S、BaSO4 蒸馏 带走水蒸气,抑制MgBr2的水解 防止倒吸 将滤液加热煮沸,向冷却后的溶液中缓慢通入SO2气体至反应液的pH约为7(用pH计测得),过滤,用溶有SO2的水洗涤滤渣,在真空干燥箱中干燥
【解析】(1) “还原”步骤中BaS与溴反应生成硫酸钡沉淀或硫沉淀,过量的BaS会与氢溴酸和硫酸反应放出硫化氢气体,因此BaS不宜过量太多,故答案为:后续反应会使用更多的H2SO4、实验过程中会产生有毒的H2S气体;
(2)根据(1)的分析,沉淀中含有硫酸钡沉淀或硫沉淀和过量的BaS,加入硫酸,将沉淀中的BaS溶解,得到的滤渣中主要含有S、BaSO4,故答案为:S、BaSO4;
(3)结晶获得的MgBr2·6H2O用乙醇洗涤,乙醇的沸点降低,可以通过蒸馏的方法从洗涤液中回收乙醇,故答案为:蒸馏;
(4)①MgBr2水解会放出溴化氢气体,通入HBr,可以带走水蒸气,抑制MgBr2的水解,故答案为:带走水蒸气,抑制MgBr2的水解;
②图中框内装置是安全瓶,可以防止倒吸,故答案为:防止倒吸;
(5)由BaS制取高纯BaSO3。取BaS加水浸出,边搅拌边在浸出液中加入过量H2O2,BaS+H2O2=Ba(OH)2+S↓,过滤除去硫,得到氢氧化钡溶液,其中含有少量过量的过氧化氢溶液,加热,使过氧化氢分解,然后在氢氧化钡溶液中通入二氧化硫气体,恰好完全反应后溶液中含有水,pH=7,过滤出BaSO3沉淀,用溶有SO2的水洗涤,在隔绝空气的环境中干燥即可,故答案为:将滤液加热煮沸,向冷却后的溶液中缓慢通入SO2气体至反应液的pH约为7(用pH计测得),过滤,用溶有SO2的水洗涤滤渣,在真空干燥箱中干燥。