题目内容
(2013?芜湖模拟)能正确表示下列反应的离子方程式是( )
分析:A.氢氧化钡和少量硫酸氢钠反应生成硫酸钡、氢氧化钠和水;
B.次氯酸能把亚硫酸钙氧化生成硫酸钙;
C.硫氢根离子水解生成硫化氢和氢氧根离子;
D.稀硝酸具有强氧化性,能把亚铁离子氧化生成铁离子,自身被还原生成一氧化氮.
B.次氯酸能把亚硫酸钙氧化生成硫酸钙;
C.硫氢根离子水解生成硫化氢和氢氧根离子;
D.稀硝酸具有强氧化性,能把亚铁离子氧化生成铁离子,自身被还原生成一氧化氮.
解答:解:A.氢氧化钡和少量硫酸氢钠反应生成硫酸钡、氢氧化钠和水,离子方程式为:Ba2++OH-+H++SO42-=BaSO4↓+H2O,故A错误;
B.次氯酸能把亚硫酸钙氧化生成硫酸钙,离子反应方程式为:Ca2++ClO-+H2O+SO2═CaSO4↓+2HCl,故B错误;
C.硫氢根离子水解生成硫化氢和氢氧根离子,水解反应离子方程式为:HS-+H2O?H2S+HO-,故C错误;
D..稀硝酸具有强氧化性,能把亚铁离子氧化生成铁离子,自身被还原生成一氧化氮,离子反应方程式为:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑,故D正确;
故选D.
B.次氯酸能把亚硫酸钙氧化生成硫酸钙,离子反应方程式为:Ca2++ClO-+H2O+SO2═CaSO4↓+2HCl,故B错误;
C.硫氢根离子水解生成硫化氢和氢氧根离子,水解反应离子方程式为:HS-+H2O?H2S+HO-,故C错误;
D..稀硝酸具有强氧化性,能把亚铁离子氧化生成铁离子,自身被还原生成一氧化氮,离子反应方程式为:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑,故D正确;
故选D.
点评:本题考查了离子反应方程式正误的判断,该知识点是高考热点,明确生成物及其性质是解本题关键,同时还要注意量的关系,易错选项是B,注意亚硫酸盐能被次氯酸氧化生成硫酸盐,为易错点.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
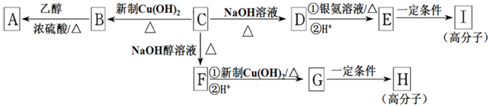



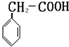 或
或 或
或 或
或
