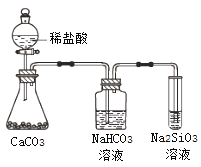
��Ŀ����
����Ŀ��I����ͼ��ʾһЩ�����е�ijЩ�ṹ�����Ƿֱ����Ȼ��ơ��Ȼ�嵐��ɱ������ʯ��ʯī�ṹ�е�ijһ�ֵ�ijһ���֣��ڵ�ɱ�ʾ��ͬ����ͬ�����ӣ���
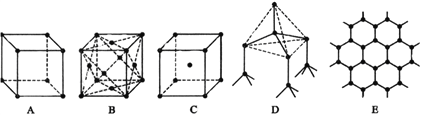
��1�����д������ʯ����_______��������ĸ����ͬ�������ʯ��ÿ��̼ԭ����_____��̼ԭ����ӽ��Ҿ�����ȡ�
��2�����д���ʯī����______������ÿ����������ռ�е�̼ԭ����ƽ��Ϊ____________����
��3�����б�ʾ�Ȼ��Ƶ���______��ÿ����������Χ������ӽ��Ҿ�����ȵ���������______����
��4�������Ȼ�蘆���________��ÿ���������________�������ӽ��ڣ�
II����1����֪14gCO��������������ȫȼ�տɷų�141.5 kJ��������д��COȼ�յ��Ȼ�ѧ����ʽ______________________________________________��
��2�������е�����ɽ�������H2S��������Ӧ������SO42����������Ӧ�������仯ʾ��ͼ���£���1mol H2S��g��ȫ��������SO42����aq�����Ȼ�ѧ����ʽΪ____________________________��
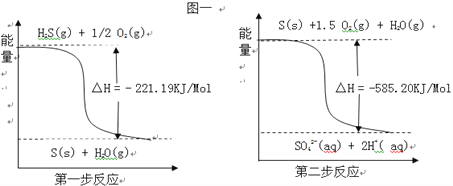
���𰸡� D 4 E 2 A 12 C 8 2CO(g) + O2(g) == 2CO2(g) ��H2 =��566.0 kJ��mol-1 H2S��g��+2O2��g��=SO42����aq��+2H+��aq����H=��806.39 kJmol��1
��������I�����⿼�鳣�����־���ľ�������1�����ʯ����ԭ�Ӿ��壬������������ʽ��������Ŀռ���״�ṹ����DΪ���ʯ�ṹ�����ʯ�����У�ÿ��̼ԭ�����ĸ����۵����ԳƵ������ڵ�4��̼ԭ�ӽ�ϣ���ÿ��̼ԭ����4��̼ԭ����ӽ��Ҿ�����ȣ���2��ʯī�Dz�״ƽ����Ԫ�����ṹ����BΪʯī�Ľṹ��ÿһ��̼ԭ�ӱ�3����Ԫ�����ã����ݾ�̯��������һ����Ԫ���ĵ�̼ԭ��ƽ��Ϊ6��1/3=2����3���Ȼ����������Ӿ��壬��ʾ�Ȼ��ƽṹ����A�������Ȼ��Ƶľ�������Na������Ҿ�����ȵ�������ͬ����4�����ϲ���4�����²���4�������������Ҿ�����ȵ�Na���ĸ���Ϊ12������4���Ȼ��Ϊ���Ӿ��壬Cs��λ�ھ����ڲ�����ʾ�Ȼ�綠ṹ����C��Cs��λ�����ģ�Cl��λ��8�����㣬���ÿ��Cs����8��Cl�����ڣ�II�����⿼���Ȼ�ѧ��Ӧ����ʽ����д����1��1molCOȼ��ʱ�ų�������Ϊ![]() kJ=283kJ�����COȼ�յ��Ȼ�ѧ��Ӧ����ʽΪCO(g)��1/2O2(g)=CO2(g) ��H=��2283kJ��mol��1��2CO(g)��O2(g)=2CO2(g) ��H=��566.0kJ��mol��1����2�����ø�˹���ɣ���Ӧ��ֻ��ʼ̬����̬�йأ��뷴Ӧ;���أ����H2S��g��+2O2��g��=SO42����aq��+2H+��aq����H=(��221.19��585.20)kJ��mol��1=��806.39 kJmol��1��
kJ=283kJ�����COȼ�յ��Ȼ�ѧ��Ӧ����ʽΪCO(g)��1/2O2(g)=CO2(g) ��H=��2283kJ��mol��1��2CO(g)��O2(g)=2CO2(g) ��H=��566.0kJ��mol��1����2�����ø�˹���ɣ���Ӧ��ֻ��ʼ̬����̬�йأ��뷴Ӧ;���أ����H2S��g��+2O2��g��=SO42����aq��+2H+��aq����H=(��221.19��585.20)kJ��mol��1=��806.39 kJmol��1��

 ����5��2���ϵ�д�
����5��2���ϵ�д�