题目内容
为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3)。碘酸钾和碘化钾在溶液中能发生下列反应:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O
(1)该反应中,氧化剂是________,氧化产物是______;
(2)当有1 mol I2生成时,有________ mol还原剂被氧化;
(3)当有1 mol氧化剂参与反应时,转移电子的数目为________。
(1)KIO3, I2 (2)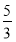 (3)5NA
(3)5NA
【解析】
试题分析:(1)该反应KIO3+5KI+3H2SO4===3I2+3K2SO4+3H2O中,碘化钾中碘元素的化合价从-1价升高到0价,失去1个电子,被氧化。碘酸钾中碘元素的化合价从+5价降低到0价,得到电子,被还原,因此氧化剂是KIO3,氧化产物是I2。
(2)根据方程式可知,每生成3mol单质碘,反应中转移5mol电子,被氧化的还原剂是5mol,所以当有1 mol I2生成时,有 mol还原剂被氧化.
mol还原剂被氧化.
(3)碘酸钾在反应中得到5个电子,所以当有1 mol氧化剂参与反应时,转移电子的数目为5NA。
考点:考查氧化还原反应的有关判断和计算

练习册系列答案
相关题目