题目内容
某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸 ②Na+水 ③Al+NaOH溶液。为点燃上述三个反应生成的H2,他们设计了如下装置(图1),请回答下列问题:
(1)写出Na与H2O反应的化学方程式_____________________________________。
(2)在点燃H2前必须先进行_____________________________________________,
方法是 _______________________________________________________。
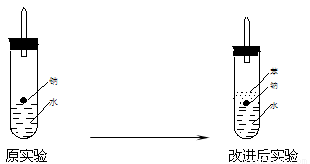
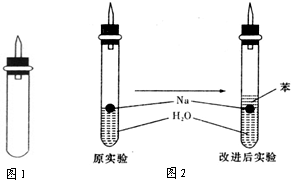
 (3)实验小组在点燃用图1装置制得的H2时,①③实验获得成功,②却失败了。他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量太少。于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因是________________________________________________________________________。
(3)实验小组在点燃用图1装置制得的H2时,①③实验获得成功,②却失败了。他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量太少。于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因是________________________________________________________________________。
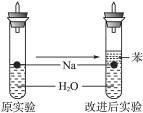
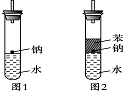
(4)实验小组查阅钠、苯、水的密度分别为0.97 g·mL-1、0.88 g·mL-1、1.00 g·mL-1,并据此对实验进行了改进(如图2),在改进后的实验中H2的生成速率减慢。原因是________________________________________________________________________。
(1)2Na+2H2O===2NaOH+H2↑
(2)检验H2的纯度用向下排空气法收集一试管氢气,用拇指堵住,移近酒精灯火焰处,移开拇指点火,如听到尖锐的爆鸣声,说明不纯,直到听到轻微的“噗”声,证明已经较纯净
(3)大块的钠与水反应剧烈,放出大量的热,可能使试管内H2和O2的混合气点燃而爆炸
(4)钠处于苯和水的交界处,钠与水反应产生的H2使钠浮起,脱离水面,反应停止;当钠表面的H2逸出,钠又回落水层,如此反复,间歇与水反应
解析:
注意试题所渗透的安全意识。

 某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸;②Na+水;③Al+NaOH溶液.为点燃上述三个反应生成的H2,他们设计了如图所示的装置图:
某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸;②Na+水;③Al+NaOH溶液.为点燃上述三个反应生成的H2,他们设计了如图所示的装置图: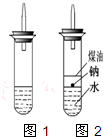 某实验小组对中学课本中已经学过的生成氢气的反应进行了研究,写出了如下三个可生成氢气的反应:
某实验小组对中学课本中已经学过的生成氢气的反应进行了研究,写出了如下三个可生成氢气的反应: