题目内容
【题目】X、Y、Z、W、R、Q是原子序数依次增大的前20号元素。X2是通常状况下密度最小的气体;Z与R同主族,R的一种固体单质在空气中易自燃;Y、W最外层电子数之和是Z的2倍,W有W2、W3两种常见单质;含Q的化合物焰色反应呈紫色。请回答下列问题:
(1)X、W、R、Q原子半径由大到小的顺序是(写元素符号)__________;请写出Z在周期表中的位置____________________。
(2)由上述元素组成的物质YW(ZX2)2是一种中性肥料,请写出它的电子式______________。
(3)请设计实验比较Z与R元素的非金属性强弱____________________。
(4)X、Y形成的化合物中含有非极性键且相对分子质量最小的物质是________。(写化学式)
(5)R的简单氢化物具有强还原性,将其通入硫酸铜溶液能生成两种最高价含氧酸和一种单质,请写出该反应的化学方程式__________________________________________________。
(6)Y的最高价氧化物与Q的最高价氧化物的水化物按物质的量之比1:2反应,所得溶液中离子浓度由大到小的顺序____________________。
【答案】K>P>O>H 第二周期ⅤA族 ![]() 配制等浓度的磷酸和硝酸溶液,分别测量其pH,磷酸溶液的pH大,说明硝酸的酸性强,即P的非金属性弱于N C2H2 4CuSO4+PH3+4H2O=4Cu↓+H3PO4+4H2SO4 c(K+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
配制等浓度的磷酸和硝酸溶液,分别测量其pH,磷酸溶液的pH大,说明硝酸的酸性强,即P的非金属性弱于N C2H2 4CuSO4+PH3+4H2O=4Cu↓+H3PO4+4H2SO4 c(K+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
【解析】
X、Y、Z、W、R、Q是原子序数依次增大的前20号元素;X2是通常状况下密度最小的气体,说明X为H元素;Z与R同主族,R的一种固体单质在空气中易自燃,此单质为P4,则Z为N元素,R为P元素;Y、W最外层电子数之和是Z的2倍,W有W2、W3两种常见单质,则W为O元素,Y为C元素;含Q的化合物焰色反应呈紫色,可知Q为K元素,据此分析并结合元素周期律分析解题。
由分析知:X、Y、Z、W、R、Q依次为H、C、N、O、P、K元素;
(1)H、O、P、K原子分属四个不同周期,结合同主族元素核电荷数大,原子半径大,而同周期主族元素,核电荷数大,原子半径小的规律可知原子半径K>Na>P>S>O>H,则半径由大到小的顺序是(写元素符号) K>P>O>H;Z为N元素,核电荷数为7,其在周期表中的位置第二周期ⅤA族;
(2)由上述元素组成的尿素(CO(NH2)2是一种中性肥料,说明其为共价化合物,则它的电子式为![]() ;
;
(3)元素的非金属性越强,其最高价氧化物水化物的酸性越强,则配制等浓度的磷酸和硝酸溶液,分别测量其pH,磷酸溶液的pH大,说明硝酸的酸性强,即P的非金属性弱于N;
(4)C、H元素可组成多种烃,其中含有非极性键且相对分子质量最小的物质是乙炔,其化学式为C2H2;
(5)PH3具有强还原性,通入硫酸铜溶液能生成两种最高价含氧酸和一种单质,应为磷酸、硫酸和Cu,则发生反应的化学方程式为4CuSO4+PH3+4H2O=4Cu↓+H3PO4+4H2SO4;
(6)CO2与KOH按物质的量之比1:2反应生成K2CO3,所得溶液中CO32-分步水解,且溶液呈碱性,则溶液中离子浓度由大到小的顺序为c(K+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)。

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
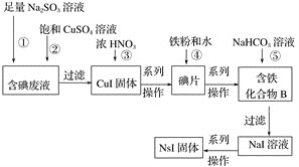
芒果教辅达标测试卷系列答案【题目】化学一选修:化学与技术磷矿石主要以[Ca3(PO4)2H2O]和磷灰石[Ca5F(PO4)3,Ca5(OH)(PO4)3]等形式存在,图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸,图(b)是热法磷酸生产过程中由磷灰石制单质磷的流程:
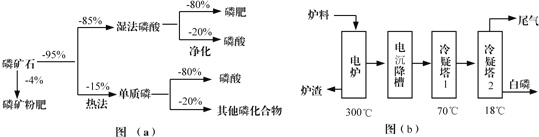
部分物质的相关性质如下:
熔点/℃ | 沸点/℃ | 备注 | |
白磷 | 44 | 280.5 | |
PH3 | -133.8 | -87.8 | 难溶于水、有还原性 |
SiF4 | -90 | -86 | 易水解 |
回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的____________;
(2)以磷矿石为原料,湿法磷酸过程中Ca5F(PO4)3反应的化学方程式为:___________,现有1t折合含有P2O5约30%的磷灰石,最多可制得到85%的商品磷酸___________t。
(3)如图(b)所示,热法磷酸生产过程的第一步是将SiO2、过量焦炭与磷灰石混合,高温反应生成白磷,炉渣的主要成分是___________(填化学式),冷凝塔1的主要沉积物是___________,冷凝塔2的主要沉积物是___________。
(4)尾气中主要含有___________,还含有少量的PH3、H2S和HF等.将尾气先通入纯碱溶液,可除去___________;再通入次氯酸钠溶液,可除去___________(均填化学式)。
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是___________。