题目内容
【题目】己二酸主要用于生产尼龙66盐、合成树脂及增塑剂等。已二酸的合成路线如下:

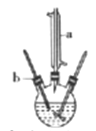
制备己二酸的装置示意图如图所示(加热和夹持装置等略)。
实验步骤:
I.己二酸的制备
连装好装置后,通过瓶口b慢慢滴加1.5g环已醇至适量KMnO4和NaOH的混合溶液中,然后塞上带有温度计的胶塞,再用沸水浴加热数分钟。
II.分离提纯
趁热过滤,收集滤液,用少量热水洗涤滤渣2次,合并滤液和洗涤液,边搅拌边滴加浓盐酸至溶液呈强酸性,小心加热蒸发浓缩至10mL左右,在冷水浴中冷却,析出已二酸粗品。
回答下列问题:
(1)写出仪器a的名称:______________。
(2)分离提纯过程中滴加的浓盐酸的作用是______________。
(3)将已二酸粗品提纯的方法是_______________。
A.过滤 B.萃取 C.重结晶 D.蒸馏
(4)步骤II中过滤时需要用到的玻璃仪器有玻璃棒____、_____。洗涤滤渣的目的是__________。
(5)若制得纯已二酸的质量为1.5g,则己二酸的产率为__________。
【答案】 直形冷凝管(或冷凝管) 将己二酸钠完全转化为己二酸 C 烧杯 漏斗 减少己二酸钠的损失,提高己二酸的产量 68.5%
【解析】(1)根据实验装置图及常见的仪器分析;
(2)根据己二酸的酸性弱于盐酸分析;
(3)根据已二酸常温下为固体,温度较低时会从溶液中析出分析;
(4)根据过滤操作分析;滤渣中含有己二酸钠;
(5)根据实际产量与理论产量的比值计算产率。
(1)由实验装置图可知,图中仪器a的名称是直形冷凝管(或冷凝管);
(2)浓盐酸是强酸,酸性强于己二酸,分离提纯过程中滴加的浓盐酸的作用是将己二酸钠完全转化为己二酸;
(3)因为己二酸常温下为固体,温度较低时会从溶液中析出,所以将已二酸粗品提纯的方法是重结晶,答案选C;
(4)步骤II中过滤时需要用到的玻璃仪器有玻璃棒、烧杯和漏斗;滤渣中含有己二酸钠,因此洗涤滤渣的目的是减少己二酸钠的损失,提高己二酸的产量;
(5)根据原子守恒可知生成己二酸的质量为![]() ,所以产率是1.5g/2.19g×100%=68.5%。
,所以产率是1.5g/2.19g×100%=68.5%。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案