题目内容
【题目】I.现有右图所示裝置,为实现下列实验目的,其中应以a端作为入口的是__________。
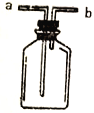
A.瓶内盛碱石灰,用以干燥气体
B.瓶内盛饱和食盐水,用以除去Cl2中混有的少量HCl
C.瓶内盛水,用以测量某难溶于水的气体体积
D.瓶内贮存气体,加水时气体可被排出
E.收集密度比空气大的气体
F.收集密度比空气小的气体
Ⅱ.欲用98%的浓硫酸(密度为1.84g·cm3)配制浓度为1mol/L的稀硫酸480mL。
(1)需取用浓硫酸的体积为______________mL(结果保留一位小数)
(2)下列情况中,会使所配溶液的浓度偏低的是__________。
A.将量筒中的浓硫酸转入烧杯后,用水洗涤量筒,将洗液也转入烧杯中
B.稀释浓硫酸后立即转入容量瓶
C.定容时加水不慎超过刻度线
D.定容时仰视刻度线
(3)容量瓶在使用前,首先应检查___________________。
(4)此实验中,玻璃棒的两个作用分别是_________、_____________________。
【答案】 BDE 27.2 CD 是否漏水(或漏液) 搅拌 引流
【解析】I.A.盛液体干燥剂,用于干燥气体时,要长进短出,但不能盛碱石灰固体干燥剂,A错误;B.瓶内盛液体洗剂,采用长进短出,可以用于除去某气体中的杂质,B正确;C.装置中预先盛满水,将水排出测量气体体积,实际上是排水法收集气体;气体从b端进入后,使瓶内压强增大,从而将其中的水排出瓶外,瓶内便收集到了所需气体,C错误;D.瓶内贮存气体,从a长导管加入水,气体能够从b短导管排出,D正确;E.收集气体从a端进入集气,实际上是向上排空气法收集气体;因此该气体必须具有的性质是:气体的密度比空气的大,E正确;F.根据E可知,从a端进入集气,气体的密度比空气的大,F错误;答案选BDE;
II.(1)配制480mL溶液,应该选用500mL容量瓶;98%的浓硫酸(密度为1.84g·cm3)的物质的量浓度为:1000×1.84×98%/98mol·L-1=18.4mol/L,配制500mL 1mol/L的稀硫酸,需要浓硫酸的体积为:1mol/L×0.5L/18.4mol/L≈0.0272L=27.2mL;(2)A.将量筒中的浓硫酸转入烧杯后,用水洗涤量筒,将洗液也转入在烧杯中,量筒不能洗涤,否则配制的溶液中溶质的物质的量偏大,根据c=n/V可得,配制的溶液浓度偏高,A错误;B.稀释浓硫酸后立即转入容量瓶,热的溶液体积偏大,冷却后溶液的体积偏小,根据c=n/V可得,配制的溶液浓度偏高,B错误;C.定容时加水不慎超过刻度线,导致配制的溶液体积偏大,根据c=n/V可得,配制的溶液浓度偏低,C正确;D.定容时仰视刻度线,导致配制的溶液体积偏大,根据c=n/V可得,配制的溶液浓度偏小,D正确;答案选CD;(3)容量瓶在使用前,首先应检查是否漏水(或漏液)。(4)此实验中,玻璃棒的两个作用分别是稀释时搅拌,转移时引流。

 阅读快车系列答案
阅读快车系列答案